Indledning
Coagulase-negative stafylokokker (CoNS), medlemmer af stafylokokker gruppe, der er karakteriseret som Gram-positive kokker, der præsenteres som enkelt celler eller med uregelmæssige disposition, og er immobilt, ikke-sporedannende, katalase-positive, for det meste valgfri anaerobes, og mangler det enzym, coagulase.,1 ulemper er en del af den humane mikrobiota, der betragtes som opportunistiske patogener, hvilket forårsager infektioner mest hos premature babyer og immunkompromitterede og protetiske patienter.2
stigningen i antimikrobiel resistens i de senere år har haft stor indflydelse på hospitalsinfektioner forårsaget af ulemper. O .acillin er et semisyntetisk penicillin, der anvendes i følsomhedstesten til påvisning af methicillinresistens og behandling af stafylokokinfektioner. Der er dog observeret satser fra 66% til 95% af O .acillinresistens I CoNS kliniske isolater.,2 O .acillinresistens medieres ofte af mecA-genet, der koder for et supplerende penicillinbindende protein (PBP2a) med lav affinitet til semisyntetiske penicilliner.3 De mecA genet ligger på et mobilt genetisk element kendt som Stafylokokker Kassette Kromosom mec (SCCmec), som indeholder mec kompleks, der består af mecA genet og dets regulator gener mecI og mecRI, modpartsrisiko-kompleks, der er ansvarlig for integration og excision af SCCmec, og J-regionen, som ikke er nødvendige for SCCmec formation, men kan udføre ikke-β–lactam-resistens-gener.,4 til dato er 13 sccmec-typer blevet beskrevet, baseret på kombinationen af CCR-genkomplekstyper og MEC-genkompleksklasser. Undertyperne blev defineret af J-regionspolymorfier i den samme kombination af MEC-og ccr-komplekser.5
fremkomsten af O .acillinresistente isolater har ført til den ultimative anvendelse af alternative antimikrobielle stoffer til behandling af CoNS-infektioner, såsom glycopeptidet vancomycin. I mellemtiden er der rapporteret beskrivelser af reduceret følsomhed og resistens over for vancomycin i de seneste årtier.,6 reduceret følsomhed over for vancomycin kan være relateret til metaboliske modifikationer, såsom acceleration i peptidoglycan-syntese, hvilket resulterer i cellevægsfortykning. I denne proces er vancomycin ikke i stand til at hæmme peptidoglycan-syntesen, da den er udtømt på grund af den højere tilgængelighed af D-alanyl-D-alanin-steder.,7
i Betragtning af den voldsomme stigning i hospital infektioner forårsaget af Ulemper, denne undersøgelse havde til formål at karakterisere oxacillin-resistente stammer og bestemme antimikrobiel følsomhed af en 20-års indsamling af blod kultur Ulemper isolater fra Botucatu Hospital das Clínicas indlagte patienter.
materiale og metoderstammer
tre hundrede CoNS stammer blev isoleret fra blodkulturer fra indlagte patienter på Botucatu Hospital das Cl .nicas-Paulista State University (UNESP)., Isolaterne blev indsamlet fra 1990 til 2009 og opbevaret i Kultursamlingslaboratoriet for Mikrobiologi og Immunologi afdeling af Botucatu Biosciences Institute – UNESP. Udvælgelseskriterierne betragtede en gennemsnitlig forekomst af hændelser på 35% med en fejlmargin på 5% og et 95% konfidensinterval.
stammerne blev isoleret ifølge Koneman et al.8 blod-agarisolater blev underkastet gramfarvning til observation af kolonimorfologi, og katalasetesten blev udført til bekræftelse af slægten Staphylococcus., Stafylokokstammer blev sendt til koagulasetesten for differentiering af de koagulase-negative og koagulase-positive grupper. Coagulase-negative isolater blev underkastet biokemiske tests til fænotypisk identifikation af arter. Den genotypiske identifikation blev udført under anvendelse af primere trukket over konserverede sekvenser ved siden af 16S-og 23S-gener ved hjælp af dens-PCR (intern transkriberet spacer–polymerasekædereaktion), beskrevet af Couto et al.9 Amplifikationseffektivitet blev overvåget ved elektroforese i 3% metafor agarose og farvet med SYBR Safe., The following lineages of international reference were used: S. auricularis ATCC 33753, S. capitis subsp. capitis ATCC 27843, S. capitis subsp. urealyticus ATCC 49325, S. caprae ATCC 35538, S. cohnii ATCC 49330, S. cohnii subsp. cohnii ATCC 29974, S. epidermidis ATCC 12228, S. epidermidis ATCC 35983, S. hemolyticus ATCC 29970, S. hominis ATCC 27844, S. hominis subsp. novobiosepticus ATCC 700237, S. lentus ATCC 700403, S. lugdunensis ATCC 700328, S. saprophyticus ATCC 15305, S. schleiferi subsp. schleiferi ATCC 43808, S. sciuri subsp. sciuri ATCC 29062, S. simulans ATCC 27851, S., 2ylosus ATCC 29979, og S. 10arneri ATCC 10209.
DNA-ekstraktion
Illustra-kittet (GE Healthcare) blev brugt til DNA-ekstraktion. Trinnene omfattede en indledende fordøjelse af stafylokokceller med Lyso .ym (10 mg/mL) og proteinase K (20 mg/mL). Dernæst blev 500ll af ekstraktionsbufferen sat til blandingen, som blev centrifugeret ved 10.000 GG I 4min. Supernatanten blev overført til en søjle og centrifugeret ved 5.000 g i 1min. Væsken blev kasseret og 500ll ekstraktion buffer blev sat til kolonnen., Efter centrifugering og kassering af den opsamlede væske blev 500ll vaskebuffer sat til søjlen, som blev underkastet centrifugering ved 20.000 g i 3min. Derefter blev kolonnen overført til et 1, 5 mL rør, og eluering blev udført under anvendelse af 200ll opvarmet Milli.vand ved 70. C.
Meca-genetektion
PCR blev udført til påvisning af mecA-genet. Reaktioner blev udført under anvendelse af en protokol beskrevet af Murakami et al.10 amplifikationseffektiviteten blev overvåget ved elektroforese i en 2% agarosegel farvet med SYBR Safe.,
bestemmelse af sccmec
sccmec-typen blev bestemt på mecA-positive stammer. Reaktioner blev udført under anvendelse af en protokol beskrevet af Oliveira et al.11 og modificeret af Machado et al.12
multiple.PCR blev udført i 50µL reaktionsvolumen med 1. en .ymbuffer, 1.,25 U Taq polymerase DNA, 200 μM dNTP Mix, and the following primers: 10pmol of RIF2 F2 (TTCGAGTTGCTGATGAAGAAGG) and CIF2 R2 (ATTTACCACAAGGACTACCAGC), 6pmol of KDP F1 (AATCATCTGCCATTGGTGATGC) and KDP R1 (CGAATGAAGTGAAAGAAAGTGG), 5pmol of DCS F2 (CATCCTATGATAGCTTGGTC) and DSC R1 (CTAAATCATAGCCATGACCG), 5pmol of RIF4 F3 (GTGATTGTTCGAGATATGTGG), and RIF4 R9 (CGCTTTATCTGTATCTATCGC). For each reaction, 10μL DNA was added. The cycle sequencing reactions were performed at 92°C for 3min, followed by 30 cycles of 92°C for 1min, 56°C for 1min, and 72°C for 1min and 30s., Forstærkningseffektiviteten blev overvåget ved elektroforese i en 2% agarosegel farvet med SYBR Safe.
Bestemmelse af den mindste hæmmende koncentration (MIC) ved E-test
in vitro-følsomhed af Ulemper stammer blev testet for følgende antibiotika: Oxacillin, Vancomycin, Daptomycin, Linezolid, Quinupristin/Dalfopristin, og Tigecycline. MIC af disse lægemidler blev bestemt af E-testen. Kriterierne for klassificering af følsomhed var: O Oxacillin
µg / mL (modtagelig) for CoNS, undtagen S., lugdunensis (modtagelige ≤2µg/mL og resistente ≥4µg/mL), Vancomycin µg/mL (modtagelig), 8–16µg/mL (intermediært resistente), og >32µg/mL (resistente); Linezolid ≤4µg/mL (modtagelig); Daptomycin ≤1µg/mL; Quinupristin/Dalfopristin ≤1µg/mL (modtagelig), 2µg/mL (mellemliggende), og ≥4µg/mL (resistente); Tigecycline ≤0.5 µg/mL.,13Screening test til påvisning af nedsat følsomhed over for vancomycin
for at opdage, nedsat følsomhed over for vancomycin, en screening agar-testen er udarbejdet med Brain Heart Infusion (BHI) Agar og 4µg/mL, 6µg/mL, 8µg/mL, og 16µg/mL vancomycin blev brugt. Reference stamme S. aureus ATCC 29213, der er modtagelige for vancomycin, blev brugt som en negativ kontrol, og stamme E. faecalis ATCC 51299, modstandsdygtig over for vancomycin, som en positiv kontrol. Pletter af en 2.,0 McFarland inokulum blev sat til Agarpladen og inkuberet ved 35 C C i 24 timer, og dyrkning af mindst en koloni blev betragtet som et positivt resultat.
analyse af cellevægtykkelsen
CoNS-stammerne, der præsenterede reduceret følsomhed over for vancomycin, blev sendt til transmissions-elektronisk mikroskopi til analyse af cellevægtykkelse. Stammer blev dyrket i bh-bouillon og inkuberet ved 37. C i 24 timer.i en mikrotube blev 1000ll af en CoNS-kulturbuljong centrifugeret i et minut ved 12.000 o / min. Efter kassering af supernatanten blev stammer fastgjort i en Karnovsky-opløsning (2.,5% glutaraldehyd i phosphatbuffer 0, 1 M) i fire timer. Prøver blev fjernet fra Fi theeren og vasket tre gange i fem minutter i destilleret vand. Derefter blev prøverne nedsænket i 0,5% osmiumtetroideid i 40 minutter, inden de vaskes tre gange i 10 minutter i destilleret vand. Prøver blev dehydreret under anvendelse af stigende koncentrationer af alkohol: to gange i 10 minutter i 7.,5% alkohol; to gange for 10min på 15% alkohol; to gange for 10min i 30% alkohol; to gange for 10min i 50% alkohol; tre gange i 15 min i 70% alkohol; to gange for 15min i 90% alkohol; to gange for 10min i 100% alkohol. Efter dehydrering blev stubberne monteret og prøver metaliseret. Analyserne blev udført i et elektronisk mikroskopi Tecnai Spirit Fei Company, og billederne blev opnået ved en forstørrelse på 30000..,
Resultateridentifikation af isolater
tabel 1 præsenterer kilden til CoNS-artens isolater samt de demografiske data fra patienter med bakteriæmi.
påvisning af mecA-gen og karakterisering af SCCmec bestemmelse af den minimale inhiberende koncentration (MIC)
Mic ‘ erne for de antimikrobielle stoffer, der blev anvendt til behandling af CoNS-infektioner, blev bestemt ved E-testen. O .acillinresistens blev fundet i 206 (68,7%) CoNS-stammer, og 25 var tigecyclinresistente (8,3%). Resistens over for tigecyclin blev påvist i 4, 5% af S. epidermidis, 13, 8% af S. hemolyticus, 13% af S., hominis og 11,1% S. lugdunensis. For quinuinuprisin/dalfopristin præsenterede et S. epidermidis-isolat mellemliggende resistens med en MIC på 2GG/mL og en S. epidermidis og en S. hemolyticus med mikrofoner på 3GG / mL. Den sensitivitet og specificitet af oxacillin MIC ved E-test sammenlignet med tilstedeværelsen af mecA var henholdsvis 87.4% og 82.3%.
med hensyn til CoNS-arter afslørede parameterfordelingen af MIC50 og MIC90 høje hastigheder af O .acillinresistens I S. hemolyticus., Dette var den eneste Ulemper arter, for hvilke minimal koncentration til at hæmme 50% af isolater var >256µg/mL, hvilket afspejler den store modstand sats af S. hemolyticus at oxacillin (Tabel 3).MIC-området for hvert antimikrobielt stof blev sammenlignet med sccmec-typen. Isolaterne skrevet som sccmeci præsenteret højere tigecyclin Mikrofoner og dem klassificeret som sccmecii præsenteret de højeste o .acillin Mikrofoner. Den SCCmecIV stammer, der viste den højeste MIC værdier for vancomycin, linezolid, daptomycin, og quinupristin/dalfopristin (Tabel 4).
Determination of the MIC range according to SCCmec.
| MIC range (μg/ml) | ||||
|---|---|---|---|---|
| Antimicrobial | SCCmec I | SCCmec II | SCCmec III | SCCmec IV |
| Oxacillin | 0.094≥256 | 6≥256 | 0.,125≥256 | 0.125≥256 |
| Vancomycin | 0.25–2 | 0.38–2 | 0.125–2 | 0.75–2 |
| Linezolid | 0.064–1 | 0.19–0.5 | 0.047–0.75 | 0.064–1 |
| Daptomycin | 0.016–025 | 0.016–0.094 | 0.019–0.5 | 0.047–0.75 |
| Quinupristin/Dalfopristin | 0.025–1.5 | 0.094–0.5 | 0.064–1 | 0.125–2 |
| Tigecycline | 0.016–2 | 0.023–0.75 | 0.016–0.75 | 0.,032-1 |
MIC (Minimal Hæmmende Koncentration.
En evaluering blev udført af oxacillin og vancomycin Mikrofoner over en periode på 20 år, der er inddelt i tre perioder i henhold til fordelingen af oxacillin og vancomycin MIC intervaller. For O .acillin blev der i den første periode (1990-2001) observeret højere værdier af MIC, men indikerer stadig modtagelighed., I de øvrige perioder (2002-2006 og 2007-2009) blev der observeret et fald i MIC-værdierne, hvilket stadig indikerer modtagelighed samt en stigning i modstandsraterne. Med hensyn til vancomycin, den samme vurdering påvist betydelige forskelle i de tre perioder, blandt stammer med Mikrofoner fra 0.047 µg/mL til 0,38 µg/mL og fra 0,5 µg/mL-2,0 µg/mL (Fig. 1).
Bestemmelse af den nedsatte følsomhed over for vancomycin
En vækst på 214 (71.3%) stammer blev observeret på BHI plade med 4µg/mL af vancomycin, 89 (29.7%) på pladen med 6µg/mL af vancomycin, og 8 (2.,6%) isolater på 8µg/mL vancomycinpladen. Ingen af isolaterne voksede i mediet med 16µg / mL vancomycin. Der var ingen signifikante forskelle i Mellemindkomstlande mellem stammer, der præsenteres ingen vækst på pladen suppleret med vancomycin, og dem, der voksede på 4µg/mL vancomycin plade. Blandt dem, der viste vækst på mediet med 6µg/mL vancomycin, var MIC–området 0, 5-2µg / mL. Blandt dem, der voksede på 8µg/mL vancomycin, var MIC–området 0, 75-24µg / mL. Stammerne dyrket på 8µg / mL vancomycin var fire S. epidermidis, en S. hemolyticus, to S. hominis og en S., capitis, alle modstandsdygtig over for oxacillin, og S. epidermidis og S. capitis at være bærere af SCCmec III, S. hominis af SCCmec jeg, og S. hemolyticus med ikke-skrevet SCCmec.
Analyse af den celle, vægtykkelse af stammer med nedsat følsomhed over for vancomycin
cellens væg tykkelse under celledeling blev målt i otte stammer (værdier er præsenteret i nanometer, mean±SD). De fire S. epidermidis-stammer præsenterede middelværdier af 21.66±1.4, 20.12±0.9, 24.24±1.3, og 14.20 1.3 1.3 nm. S. hemolyticus-isolatet viste en cellevægtykkelse på 24, 88.1, 7 nm. For S., capitis-isolat, cellevægtykkelsen var 19,33.1,8, og for de to S. hominis-isolater var værdierne 17,68 and 2,1 og 24,92. 1,5. Til sammenligning, den anvendte reference stammer S. epidermidis ATCC 12228 og S. hemolyticus ATCC29970 viste, at cellens væg tykkelser på henholdsvis 14.61±1.2 og 14.73±0.7 nm. Sammenligningen af de undersøgte stammer mod kontroller viste højere værdier, der spænder fra 17 nm til 24.92 nm, med undtagelse af et S. epidermidis-isolat, som præsenterede en lavere værdi sammenlignet med kontrollerne (fig. 2).,
Ulemper bakteriæmi evolution
Den mulige udvikling af bakteriæmi til andre infektioner, såsom sepsis, pneumoni, urinvejsinfektion, meningitis, peritonitis, nekrotiserende enterocolitis, omphalitis, og hjernen bylder, blev fulgt op i 52 patienter indlagt på neonatal afdelinger. Af disse blev hos 25 (46, 3%) patienter de samme ulemper isoleret fra blodkultur bekræftet at være det etiologiske middel til infektion. I seks (11,1%) var ulemper det mulige middel til infektion, og i 23 (42,6%) var ulemper ikke relateret til patientens infektion (fig. 3).,
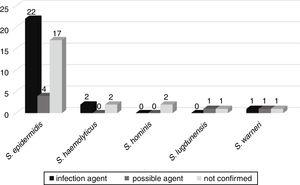
korrelation af ulemper isoleret fra blodkulturer som mulige etiologiske midler af infektioner forårsaget hos neonatale enhedspatienter.
De mecA genet blev fundet i 33 (61.1%) af disse Ulemper, med 20 (60.6%) Ulemper, der er forbundet med mere alvorlige infektioner eller potentielle agenter for disse infektioner.
Diskussion
ulemperne betragtes som en af hovedårsagerne til bakteriæmi., Betydningen af disse bakterier er steget i hospitalsmiljøet i de senere år, hovedsagelig på grund af antimikrobiel resistens. I det nuværende arbejde blev 300 CoNS-stammer isoleret fra blodkulturer af indlæggere på Hospital of Clinics of Botucatu over en periode på 20 år undersøgt. Disse isolater blev karakteriseret med hensyn til deres antimikrobielle følsomhed.
De mecA opdagelse bestemt oxacillin modstand i 78.5% af de Ulemper, og MIC50 værdi (2µg/mL) var tegn på resistens over for dette stof, der bekræfter lav modtagelighed af disse bakterier til at β–lactam-agenter., Tidligere værker har vist, at CoNS-isolaterne siden 1970 ‘ erne har præsenteret højere o .acillinresistenshastigheder end S. aureus.14,15 β-lactam resistens satser har vist sig at variere fra 65% til 95% på hospitaler i Brasilien og i andre lande.2,16,17 De højeste satser af oxacillin resistens blev fundet i S. epidermidis, efterfulgt af S. hemolyticus, S. hominis, og S. capitis. Lignende resultater blev beskrevet i tidligere undersøgelser, der viste o epidacillinresistens hos 97% af S. epidermidis mellem 1999 og 2001 i en neonatal intensivafdeling(NICU), 18 i 96% af S., hemolyticus isoleret i Brasilien,19 og i 100% af S. hominis isoleret i en NICU fra Spanien.20 vedrørende S. capitis blev der fundet uoverensstemmende resultater i undersøgelserne udført af Caier .o et al.21
skønt mecA-genet ved en lavere frekvens blev påvist i S. andarneri og S. lugdunensis. S. warneri er blevet beskrevet med priser på 33,3% af oxacillin modstand i NICUs,22 og den første beskrivelse af mecA i S. lugdunensis var i den undersøgelse af Kawaguchi et al.23 på trods af de lave resistenshastigheder,24 bestemmelse af antimikrobiel følsomhed af S., lugdunensis er vigtig, ikke kun på grund af dets kliniske implikationer, da denne art er den mest aggressive af ulemperne, men også for etablering af tidlig behandling med passende antimikrobielle stoffer og gode kliniske resultater.25
karakteriseringen af sccmec viste tilstedeværelsen af type I-IV i isolaterne, hvor sccmeciii var den hyppigst detekterede i de undersøgte stammer, hovedsageligt i S. epidermidis, den eneste art, der bar type IV., SCCmec type III er den største af dem alle, kodificerer for flere resistensassocierede gener, og er de mest almindeligt isolerede ulemper fra hospitalsprøver. S. epidermidis er den vigtigste kolonisator af den menneskelige hud og den mest almindeligt detekterede på infektionssteder. Det selektive Tryk i hospitalsmiljøet fører til spredning af sccmec III-stammer, der er forbundet med alvorlige infektioner.26 sccmec type IV har været beslægtet med Staphylococcus spp., og blev beskrevet for første gang i en S. epidermidis-stamme, en kendsgerning, der indebærer dens overførsel fra S., epidermidis til S. aureus. En reduceret omkostningsoverførsel af sccmec IV på grund af dens lille størrelse ville sandsynligvis føre til en højere forekomst af infektioner forårsaget af sccmec IV-bærere.12,27 sccmecii præsenterede en forening med S. hemolyticus, svarende til resultaterne af Machado et al., 12 hvis arbejde kun detekterede type II i denne art.
alternativet til behandling af O .acillinresistente stafylokokker er vancomycin, et glycopeptid, der først blev anvendt i 1958 i invasive infektioner. Der er imidlertid beskrivelser af resistens og reduceret modtagelighed for dette lægemiddel,6 selvom det er ustabilt.,28 resultaterne af det nuværende arbejde viste, at vancomycin med undtagelse af O .acillin var lægemidlet med de højeste værdier af MIC50 og MIC90. På trods af samlingens fulde modtagelighed var MIC-værdierne de højeste i perioden 20 år, og reduceret modtagelighed blev påvist i nogle S. epidermidis, S. hemolyticus, S. hominis og S. capitis stammer. I undersøgelserne udført af Natoli et al.Blev 29 reduceret modtagelighed for vancomycin påvist med en frekvens på 5, 4% blandt CoNS-isolater i S. epidermidis og S. hemolyticus-arter., Ifølge de samme forfattere kan Staphylococcus kolonier dyrket på vancomycin agar føre til glycopeptid heteroresistance, som kan være en forløber for glycopeptidresistens, hvilket forårsager komplicerede infektioner og behandlingssvigt. Dette bør tages i betragtning ved terapeutiske beslutninger.30
stigningen i andelen af O .acillinresistente ulemper og fald i deres modtagelighed for vancomycin understreger vigtigheden af undersøgelser, der involverer andre terapeutiske valg., Tigecycline, Gram-positive og negative bredt spektrum semisyntetisk glycylcycline, anses et stof med fremragende aktivitet mod oxacillin modtagelige og resistente Ulemper,14,29 på trods af vores data viser priser på 8,3% af modstand, oftest i S. hemolyticus, efterfulgt af S. hominis, S. lugdunensis, og S. epidermidis. Lignende MIC90-resultater blev beskrevet for tigecyclin uden forskel mellem o .acillinresistente og modtagelige ulemper.31 i undersøgelserne udført af Natoli et al.29 tigecyclin viste god aktivitet mod ulemper., Ifølge disse forfattere anbefales tigecyclin ikke til behandling af bakteriæmi, og dets anvendelse bør begrænses for at bevare aktivitet mod multiresistente Gram-negative bakterier. Mutationer i det ribosomale gen S10 og rpsJ og mepA synes at være forbundet med tigecyclinresistens.32,33
Quinuinupristin / dalfopristin er et streptogramin tilhørende makrolid-lincosamid-streptogramin-gruppen., Kombinationen af quinuinupristin og dalfopristin er synergistisk og sædvanligvis bakteriedræbende, når disse midler sammenlignes enkeltvis eller sammenlignet med lignende makrolid antimikrobielle stoffer.34 i dette arbejde blev der på trods af fremragende effektivitet hos størstedelen af de undersøgte ulemper påvist mellemresistens over for dette lægemiddel i to S. epidermidis og en S. hemolyticus. I undersøgelsen udført af Mendes et al.,35 quinupristin/dalfopristin demonstreret fremragende effektivitet for Ulemper, de stammer, der var fuldt modtagelige, med MIC90 værdier på 0,38 µg/mL for oxacillin-modtagelige stammer og 0.,75µg / mL for de o .acillinresistente stammer. Derudover Venkatesh et al.36 beskrevet god effektivitet af quinuinupristin / dalfopristin for O .acillinresistente og modtagelige stammer.
Daptomycin, et antimikrobielt undersøgt i årtier, blev bragt i brug i 2006 til behandling af bakteriæmi og endokarditis forårsaget af stafylokokker.37 i den foreliggende undersøgelse viste daptomycin fremragende effektivitet for CoNS-isolater med lave MIC50-værdier. Olivares et al.37 verificerede også følsomheden af alle ulemper over for daptomycin med lav variation i MIC-værdierne., I et værk, der studerer 1126 ulemper, udført af Critchley et al.,38 daptomycin var aktiv på en MIC spænder fra 0.015-2,0 µg/mL, og MIC90 0,5 µg/mL. Ifølge disse forfattere var de mest aktive stoffer i disse analyser daptomycin og daluinupristin / dalfopristin, hvilket understreger relevansen af disse antimikrobielle stoffer til behandling af infektioner forårsaget af ulemper.
Line .olid, et syntetisk o .a .olidinon, der potentielt er aktivt mod flere bakterier, er et andet lægemiddel, der har vist god effektivitet mod ulemper.,39 Line .olid er blevet vigtig for terapeutisk behandling af kroniske infektioner ved ulemper, på trods af beskrivelsen af resistens. I Brasilien er det første tilfælde af linezolid modstand blev beskrevet i 2006, på en klinisk isolat af MRSA40 og blandt de Ulemper, i S. epidermidis, S. hominis, og S. hemolyticus.41 i arbejdet udført af Olivares et al., 37 på trods af påvisning af syv line .olid-resistente stammer præsenterede dette lægemiddel effektive MIC-værdier i CoNS-stammer. På den anden side et udbrud af Line S.olid resistent S., epidermidis-kloner indeholdende mutationer i ribosomale proteiner L3 og L4 samt cfr-plasmidet, der for nylig blev identificeret i Frankrig, er blevet rapporteret.42
S. hemolyticus var den art, der præsenterede de højeste O .acillin MIC-værdier, og koncentrationer højere end 256µg / mL var nødvendige for at hæmme 50% af isolaterne. Ud over o .acillin præsenterede denne art højere MIC-værdier for tigecyclin og de fleste af de testede antimikrobielle stoffer. Flere værker viser høj resistens over for de antimikrobielle stoffer, der anvendes til behandling af infektioner forårsaget af S., hemolyticus, især methicillin og glycopeptider. Nogle forfattere beskriver en høj forekomst af gener, der koder for resistens over for β-lactam-og aminoglycosid agenter, samt at en betydelig del af isolater med MIC-værdier tæt på den modstand breakpoint,43,44 understreger betydningen af S. hemolyticus som en multiresistent patogen.
foreningen af MIC område med SCCmec typer påvist højere Mikrofoner for vancomycin, linezolid, daptomycin, og quinupristin/dalfopristin i S. epidermidis, der transporterer SCCmecIV., Generne relateret til resistens over for disse antimikrobielle stoffer medieres af plasmider, der hovedsageligt findes i methicillinresistente stammer med hospitalsoprindelse.45 SCCMEC IV er karakteristisk for samfundsisolater, især på grund af dens størrelse og lave adaptive omkostninger. Undersøgelser antyder, at erhvervelsen af resistensgener har miljømæssig ikke-klinisk oprindelse i betragtning af den høje mangfoldighed af resistensgenbærere i det naturlige miljø.46,47 Desuden blev SCCmecIV kun påvist i S. epidermidis, som som den mest almindelige art i menneskelig hud er mest påvirket af selektivt tryk., Den højere Mellemindkomstlande i forhold til andre antimikrobielle stoffer kan også være relateret til det selektive pres, så omfanget af eksponering for disse stoffer i hospitalsmiljøet ville bias i udvælgelsen af nedsat modtagelighed og resistente stammer, da flere mutation begivenheder, genetisk rekombination, og ændringer i mikrobiel fysiologi er nødvendige for at generere fænotypiske ændringer.,48
metaboliske og fysiologiske modifikationer relateret til selektivt tryk kunne observeres i stammer dyrket på 8µg / mL vancomycin agar, da cellevægsfortykkelsen blev fundet i de fleste CoNS-isolater på grund af øget peptidoglycan-syntese. Denne mekanisme er mere fordelagtig for ulemper end erhvervelsen af van operon, som er en mediator af vancomycinresistens. Van operon erhverves ved vandret genoverførsel, og dens ekspression stimuleres kun i nærvær af glycopeptid., Denne stimulus medfører en meget høj adaptiv pris i nærvær af vancomycin, hvilket er ufordelagtigt for ulemperne i et vancomycinmedium.48,49 med hensyn til erhvervelse af andre resistensgener I ulemper, såsom mecA-genet, blødgøres de indledende adaptive omkostninger ved kompenserende yderligere mutationer for resistensens “omkostninger”. For nylig har punktlige mutationer i gener, såsom vraR, vist sig at være forbundet med reduceret modtagelighed for vancomycin og cellevæg fortykkelse i stafylokokker.,50
Den foreliggende undersøgelse viste, at en høj rate af bakteriæmi forårsaget af Ulemper i neonatal og pædiatriske enheder, der involverer børn under et år, er de vigtigste agenter at være S. epidermidis, S. hemolyticus, S. hominis, S. lugdunensis, og S. warneri. S. capitis blev ikke isoleret i disse enheder, idet de var agenter for bakteriæmi hos voksne indlagt på internmedicinsk afdeling, gastroenterologi, neurologi og akutrum.,da undersøgelsen involverede bakteriæmi forårsaget af stafylokokker isoleret over mere end 30 år, kunne meget af dataene i forbindelse med patienters medicinske poster ikke hentes, så det var ikke muligt at knytte infektionsresultatet af alle patienter, hvilket er en begrænsning af den aktuelle undersøgelse. Data opnået fra patienter i neonatale enheder indikerede den kliniske betydning af CoNS-bakteriæmi, som kan udvikle sig til sygdomme, der kræver specialiseret pleje.kendskab til antimikrobiel resistens er af stor betydning for korrekt behandling af infektioner forårsaget af ulemper., Desuden er virulensfaktorerne for disse bakterier og immuniteten hos patienter faktorer, der bidrager til mikroorganismens evne til at forårsage mere alvorlige infektioner.
resultaterne af vores undersøgelse, der spænder over 20 år, viste en høj frekvens af antimikrobiel resistens i ulemper, hvilket afspejler overdreven brug af disse lægemidler., Ud over de metaboliske og fysiologiske modifikationer, der kan føre til reduceret modtagelighed for antimikrobielle stoffer, gør deres tilstand som humane kommensale bakterier dem ideelle transportører og et effektivt reservoir af resistensgener, især lavpriselementerne, såsom sccmec.45 de antimikrobielle stoffer, der gav de bedste resultater, bør anvendes på en sådan måde, at de bevarer deres virkning og forhindrer resistens.,
interessekonflikter
forfatterne erklærer, at forskningen blev udført i mangel af kommercielle eller økonomiske forhold, der kunne fortolkes som en potentiel interessekonflikt.