Johdanto
Posteriorinen palautuva enkefalopatia-oireyhtymä (PRES), ensimmäinen kuvattu Hinchey ym. vuonna 1996, on neurologinen häiriö monipuolinen kliininen kuva ja tyypillinen kuvantamisen havainnot parieto-takaraivon hallitseva kuvio vasogenic turvotus (1, 2). PRES: n syitä on lukuisia dokumentoituja, ja tapaukset on ensin kuvattu kohonneiden valtimopaineiden asettamisessa., Esimerkkejä kliinisen skenaarioita, jotka PRES voidaan nähdä ovat: hypertensiivinen hätätilanne, (pre)eklampsia, munuaissairaus, autoimmuunisairaus, ja sytotoksisten lääkkeiden, muun muassa (3, 4) (Taulukko 1). PRES voi esiintyä missä tahansa ikäryhmässä ja sitä esiintyy enemmän naispotilailla (7, 8). Vaikka nykyinen kirjallisuus on suhteellisen harva verrattuna aikuisten väestöryhmiä, erityisesti on syytä mainita PRES vuonna lapsipotilailla., Lapsipotilailla on samanlainen kliininen esitys kuin aikuispotilailla, ja hypertensio, kouristuskohtaus ja psyykkisen tilan muutokset ovat yleisiä taudin ilmenemismuotoja (9). Vaikka useimmissa tapauksissa lasten PRES on raportoitu syöpäpotilailla, erityisesti post-kantasolusiirtoa potilaalle (10, 11) tutkimuksessa Gupta et al. (12) todettiin, että munuaissairaus oli ehkä yleisin PRES-taudin aiheuttaja lapsipotilaalla. Lapsipotilailla oli tutkimuksessaan epätyypillisempiä kuvantamislöydöksiä (62,5%), mukaan lukien otsalohkon osuus (56%).,
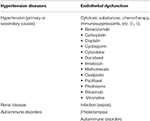
Taulukossa 1. Pres: ään liittyvät merkittävät tautitilat.
Kliiniset oireet ovat akuutti ja subakuutti ja vaihtelevat päänsärky ja näköhäiriöt muuttunut tietoisuuden tasoja ja takavarikko vaikeammissa tapauksissa (1). Hoito on yleensä suunnattu suunnattu perimmäinen syy, yleensä palautuvia, oireita ja kuvantamisen havainnot useimmissa tapauksissa (8)., Vaikka tulokset ovat yleisesti ottaen suotuisat kunnon hallinta, huono kliinisiä tuloksia on liittynyt ennestään diabetes, ja osallistuminen corpus callosum; kuitenkin, muu luotettava kuvantamisessa käytettävät biologiset merkkiaineet ennustus on tällä hetkellä puutteellista (13). Neuroradiological kuvantaminen on keskeinen rooli diagnoosi PRES tyypillinen kuvantamisen ominaisuuksia paras arvostettu magneettikuvaus (MRI) (2).
Opiskelija
tarkka pathophysiologic mekanismi(s) takana PRES ole vielä täysin selvitetty ja edelleen kiistanalainen (3)., PRES: n patofysiologiaan on tällä hetkellä kaksi merkittävää ehdotettua mekanismia (Kuva 1). Ensimmäinen teoria esittää valtimopaineiden lisääntymistä ensisijaisena tekijänä (8). Nopea nousu veren paineet lopulta voittaa autoregulatory valmiuksia aivojen verisuonistossa aiheuttaa verisuonten vuoto ja tuloksena vasogenic turvotus (14). Tiukkaliitoksen (15) kautta kulkevien proteiinien kanssa on mahdollisesti veri-aivoesteen (BBB) toimintahäiriö., Alueet toimittamien taka-liikkeeseen (nikamavaltimoiden, basilaarivaltimon, ja posterior aivovaltimoiden) ovat poikkeuksellisen riski verrattuna etuosan verenkierto (sisäinen kaulavaltimoiden, keskellä aivojen verisuonet, ja anterior aivojen valtimo), koska puute sympaattinen sävy basilaarivaltimon verisuonistossa (8)., Liittyvän teorian ehdottama joitakin oletetaan, että äärimmäinen verenpainetauti tuloksia vasospasmi ja paikallinen iskemia, joka aiheuttaa BBB erittely ja tuloksena vasogenic turvotus, kuten oli havaittu potilailla, joita hoidetaan immunosuppressiiviset lääkeaineet siklosporiini A: n ja FK-506 (16). Häiriöitä BBB aiheuttaa tyypillinen havainnot vasogenic turvotus vs. sytotoksisten turvotus (joka voi olla nähnyt asetus akuutin infarktin ja edustaa lisääntynyt solunsisäisen veden sisältöä, koska menetys tavallista osmoottinen kaltevuus asetus cell death (17).,
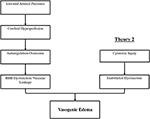
Kuva 1. Kaksi tärkeää teoriaa PRESin patofysiologiasta. Teoria 1 on hypertensiivinen ja aivojen hyperperfuusioteoria ja teoria 2 on endoteelin toimintahäiriöteoria.
toinen merkittävä teoria kohdistuu siihen, että jopa 30% potilaista, joilla PRES eivät näytteille kohonnut valtimoiden paineet tarpeen ylittää autoregulatory valvonta aivojen verisuonistossa (18, 19)., Tämä teoria ehdottaa, että endoteelin toimintahäiriö on ensisijainen syyllinen, joka voi johtua eri endogeeninen tai eksogeeninen myrkkyjä (20). Tämä teoria voi selittää havainnot PRES nähnyt potilailla, jotka saavat immunosuppressiivista lääkkeitä ja/tai kemoterapiaa, ja myös ne potilaat, joilla on sepsis (21, 22). Tässä malli, kiertävä myrkkyjä aiheuttaa verisuonten vammoja, millä kehitystä vasogenic turvotus. Endoteelivaurio aiheuttaa vasokonstriktiivisten ja immunogeenisten aineiden vapautumista edelleen, mikä voi aiheuttaa vasospasmia ja/tai verisuonten läpäisevyyden lisääntymistä., Lopulta, endoteelin toimintahäiriö, joka mahdollistaa verisuonten vuoto ja vasogenic turvotus on ajo tekijä takana PRES, riippumatta ensisijainen aivojen verisuoniston poikkeavuutta (kun kyseessä on verenpainetauti) tai toissijainen verenkierron myrkkyjä. Yhteenveto näiden kahden teorioita sekä luettelo aiemmin raportoitu chemotherapeutics ja muut immunosuppressantit on esitetty Kuvassa 2.
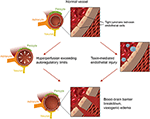
Kuva 2. Kuvituskuva kahdesta pääteoriasta, jotka koskevat PRESin taustalla olevaa patofysiologiaa., Tunnustus: kohteliaisuus Caroline O ” Driscoll, MA (hän kuvitti tämän itse ja on työntekijä yliopistomme).
Kliiniset oireet riippuvat mukana alueen(s) aivojen; näin ollen esitys voi olla laaja. Esimerkiksi takaraivolohkojen ensisijainen osallistuminen voi johtaa näköhäiriöihin / hallusinaatioihin. Fokaalisia neurologisia vajeita, jotka vastaavat fokaalisten leesioiden sijaintia, esiintyy ~5-15%: lla potilaista, joilla on PRES (23)., Harvoin selkäytimen osallistuminen voi johtaa myelopatian tai halvauksen kliinisiin merkkeihin ja oireisiin (24).
Imaging
Kuten nimestäkin voi päätellä, PRES tyypillisesti ilmenee imaging tutkimuksissa taka-hallitseva valkoinen asia vasogenic turvotus. Parietaali-ja takaraivolohkot ovat lähes yleismaailmallisesti mukana ja löydökset ovat tyypillisesti symmetrisiä ja kahdenvälisiä (1). Myös otsalohkojen, erityisesti superior frontal sulcin, osallistuminen on yleisesti nähtävissä., Vasogenic turvotus, vaikka se voi aiheuttaa aivojen harmaan aineen, on usein helpommin arvostettu toistuvia valkean aineen. CT-tutkimus on usein ensimmäinen kuvantamisen testi asetus akuutti neurologisia oireita ja voi osoittaa valkean aineen hypoattenuation kärsivillä alueilla (25) (Kuva 3: TT PRES). Kaiken kaikkiaan löydökset kuvataan parhaiten magneettikuvauksella, joka osoittaa lisääntynyttä herkkyyttä ja parempaa anatomista luonnehdintaa verrattuna CT: hen (26). Lisäksi MRI voi auttaa erottamaan muita patologisia tiloja, jotka voivat ilmetä kliinisesti samoin PRES., T2-painotteiset ja T2-FLAIR (neste-heikennettyjä inversion recovery) sekvenssit, erityisesti, ovat kaikkein hyödyllistä havaita vasogenic turvotus MK (Kuva 4: ARVOISA PRES; Kuva 5: ARVOISA PRES Koronan).
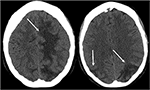
Kuva 3. Potilas, jolla on systeeminen lupus erythematosus ja nopeasti etenevä glomerulonefriitti, johon liittyy kouristuskohtaus. Ei-kontrasti CT-kuvia pään osoittaa vasogenic turvotus kahdenvälisissä päälaen ja takaraivo lohkoa, vasen suurempi kuin oikea, sekä laajennus vasempaan otsalohkoon.,
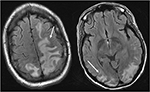
Kuva 4. Potilas, jolla on systeeminen lupus erythematosus ja nopeasti etenevä glomerulonefriitti, johon liittyy kouristuskohtaus. T2-FLAIR-kuvien pää osoittaa vasogenic turvotus kahdenvälisissä päälaen ja takaraivo lohkoa, vasen suurempi kuin oikea, sekä laajennus vasempaan otsalohkoon. Huomaa, että turvotuksen vasogeenisen kuvion vuoksi aivokuoressa säästetään signaalin poikkeavuutta.
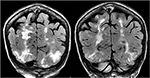
Kuva 5., Potilaan historia primaarinen myelofibroosi ja luuydinsiirron Takrolimuusin esittelee ensimmäisen kerran kohtauksen. Koronaaliset T2-FLAIR-sekvenssit osoittavat laajan signaalin poikkeavuutta kahdenvälisissä takaraivolohkoissa ja parietaalilohkoissa, kuten PRES: lle on tyypillistä.
erotusdiagnoosi PRES on laaja ja sisältää yritykset, joilla on samanlaiset yhtyviä T2 valkoinen asia hyperintensity., Esimerkkejä ovat: iskemia/infarkti (erityisesti taka-liikkeeseen), demyelinisoivat sairaudet, tarttuva etiologia (aivokalvontulehdus, enkefaliitti), progressiivinen multifokaalinen leukoenkefalopatia (PML), vaskuliitti, ja erilaiset aineenvaihdunnan häiriöt (27). Kliinisesti liittyvä kokonaisuus nimeltään palautuva aivojen verisuonten supistumista oireyhtymä (RCVS) on ajateltu olevan aiheuttamia muutoksia aivojen verisuonten sävy, mikä johtaa verisuonten supistumista., RCVS ilmenee toistuvia thunderclap päänsärky, kouristuskohtaus, aivohalvaus ja ei-aneurysmaisia subaraknoidaalinen verenvuoto (28), joka voisi olla väärässä PRES kliinisen perusteella. Tämä kokonaisuus esiintyy tyypillisesti partumin jälkeisenä aikana tai adrenergisille tai serotonergisille lääkkeille altistumisen jälkeen. RCVS voi tyypillisesti olla diagnosoitu angiografisen tutkimukset osoittavat, multifokaalinen alueilla ahtauma, johon liittyy aivojen valtimot (29). Tämä diagnoosi voidaan sekoittaa se, että RCVS ja PRES tapahtuvat usein samanaikaisesti, josta neuroradiologi pitäisi olla tietoinen välttää väärän diagnoosin (30).,
PRES voidaan tyypillisesti erottaa akuutista iskemiasta, koska jälkimmäinen osoittaa poikkeuksetta sytotoksista turvotusta ja diffuusiorajoitusta. Rajoitettu diffuusio akuutti iskemia voidaan helposti havaita diffuusio-painotettu kuvantaminen (DWI) ja näennäinen diffuusiokerroin (ADC) kuin hyperintensiivistä signaalin DWI kanssa vastaava vähentynyt signaali ADC (johtuen suhteellisen vähentynyt liikkuvuus solunsisäisen veden molekyylit)., Vasogenic turvotus asettaminen PRES, toisaalta, voi näyttää hyperintensiivistä signaalin DWI, että mukana ei ole vastaavaa vähentynyt signaali ADC (31). Lisäksi akuutti iskemia on yleensä yksipuolinen ja yksikössä verisuonten alueella. Kun arvioidaan levittämisen rajoittaminen erottaa PRES päässä iskeeminen poikkeavuus yleensä on luotettava, on olemassa harvinaisia tapauksia, PRES, jotka voivat liittyä alueilla diffuusio rajoitus päälle, kun alueita enemmän klassisesti nähnyt eristetty vasogenic turvotus.,
Pres: n”edistyneitä” kuvantamistekniikoita on viime aikoina kuvattu apuvälineenä vaikeissa tai epäselvissä tapauksissa. Nämä kehittyneet kuvantamismenetelmät ovat: CT/MR perfuusio, ARVOISA Spektroskopia (MRS), Alttius painotettu kuvantaminen (SWI), ja isotooppilääketieteen tekniikoita, mukaan lukien single-photon emission tomography (SPECT) ja positroniemissiotomografia (PET) vaihtelevalla radiotracers. Vaikka koko keskustelu ei kuulu tämän tarkastelun, erilaisia kuvantamisen havainnot voidaan nähdä näitä kehittyneitä tekniikoita, joiden avulla ehdottaa diagnoosi PRES., Hyperperfusion voidaan nähdä CT/MR perfuusio-tutkimukset osoittivat, lisäämällä aivojen verenkiertoa ja veren määrä, joilla on alentunut aika perfuusio ja keskimääräinen kuljetusaika (32) vaikka tapauksia hypoperfuusiosta on raportoitu (33). ROUVA, siellä on yleensä vähentää N-Acetylaspartate (NAA)/Kreatiini (Cr) ja NAA/Koliini (Chol) suhde, viittaavia häiriöitä normaalia synapsien ja neuroaxonal toiminto (34). SWI voi auttaa tunnistamaan verenvuodon läsnäolon PRESISSÄ, suuremmalla herkkyydellä kuin GRE-kuvantaminen (35)., SPECT/PET-kuvantamisen tyypillisesti osoittaa joko hyperperfusion tai hypoperfuusiosta (samanlainen CT/MR-perfuusio-tutkimukset), joilla on alhainen aineenvaihdunta mukaan FDG-PET (36).
Lisäksi, PRES voidaan erottaa muita ehtoja, kuten autoimmuuni enkefaliitti asettaminen akuutti disseminoitunut enkefalomyeliitti (ADEM), jonka entinen”s hajanainen kahdenvälisten mutta epäsymmetrinen vasogenic turvotus (37)., PML voi olla samanlainen ulkonäkö verrattuna PRES, ottaa parieto-takaraivon ylivalta, mutta voi olla ominaista sen enemmän yksipuolinen tai epäsymmetrinen osallistuminen, sekä mieltymys toistuvia valkean aineen (38).
Epätyypillinen Kuvantamisen Ominaisuuksia
Epätyypillisiä piirteitä PRES kuuluvat alueet, kontrasti lisälaite, verenvuoto, tai levittämisen rajoittamista (39)., Vaikka päälaen ja takaraivo lohkoa ovat yleensä mukana, epätyypillisillä alueilla osallistumisen voidaan nähdä, mukaan lukien: aivorunko, pikkuaivot, aivokurkiainen, ja muut aivojen alueet, joissa on enemmän yhteisiä alueita, mukaan lukien otsalohkojen (nähdä jopa 68%) ja huonompi ajallinen lohkoa (jopa 40%) (23, 40) (Kuva 6: Pikkuaivot; Kuva 7: Aivorunko).
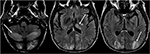
Kuva 6. Maksansiirtopotilas 6 viikkoa aiemmin. Takrolimuusin käyttö aloitettiin maksansiirron jälkeen., T2-FLAIR-kuvat aivoista osoittavat signaalin poikkeavuutta takaraivolohkoissa. Siellä on myös laaja signaali poikkeavuus nähdään kahdenvälisiä pikkuaivojen hemisfäärit ja sisällä thalami. Nämä löydökset hävisivät nopeasti takrolimuusin lopettamisen jälkeen.
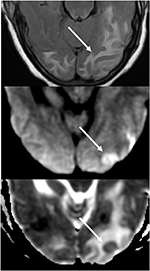
Kuva 7. Potilas, jolla on hallitsematon hypertensio, johon liittyy psyykkisen tilan muutos. T2-FLAIR (ylhäällä) kuva osoittaa turvotusta takaraivolohkoissa., DWI (keskellä) ja ADC-kartta (alhaalla) kuvia osoittaa pieni nuoli rajoitettu diffuusio, jossa hyperintensiivistä signaalin DWI ja vastaavat hypointensity on ADC-kartta.
Lisäksi, varhainen toteaminen PRES, joka voi edeltää tyypillinen parieto-takaraivon turvotus sisältää lievä sulcal HOHTO hyperintensity ja leptomeningeal lisälaite post-kontrasti T1 painotettu kuvia, kuten on kuvattu Nakagawa ym. (41). Benziada-Boudour ym., (42) kuvattu samanaikaista kehitystä sytotoksisen turvotuksen, jolloin rajoitettu diffuusio (Kuva 8: Diffuusiorajoitus). Luonnostaan taudin nimi prosessi, havainnot liittyvät PRES ovat yleensä palautuvia, normalisoituminen kliininen ja kuvantamisen havainnot kun yllyttämisestä asia on käsitelty. Kuitenkin, joissakin tapauksissa, alueet rajoitettu diffuusio voi lopulta aiheuttaa pysyviä vammoja aivoihin parenchyma (Kuva 9: Laminar Kuolio)., Verenvuoto on harvemmin nähty PRES, esiintyy 5-30% tapauksista, mutta sen pitäisi olla tunnustettu että ei ole virhe tämä havainto toisen patologinen kokonaisuus, asianmukaisessa hoitopaikassa PRES (39). Kuvantamisen havainnot verenvuoto voi sisältää: polttoväli hematooma, verenpurkaumat gyral verenvuoto, ja/tai lukinkalvonalainen verenvuoto (43) (Kuva 10: Verenvuoto).
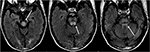
Kuva 8. Potilaan historia maksansiirto kaksi viikkoa aiemmin Takrolimuusi., T2-FLAIR-kuvissa näkyy signaalin poikkeavuus keskiaivojen, ponien ja ylivertaisten pikkuaivojen polkujen sisällä.
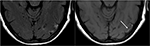
Kuva 9. T2-FLAIR (vasen) kuva potilaan hallitsematon verenpainetauti ja ennen kuvantaminen osoittaa, PRES (ks. Kuva 6), nyt hallinnassa ja 6 viikkoa myöhemmin, osoittaa, resoluutio aiemmin nähnyt turvotus. Vasemmassa ohimolohkossa on pieniä loukkaantumisesta johtuvia glioosin alueita. Aksiaalinen ei-kontrasti T1 osoittaa kaareva kortikaalinen laminaarinen nekroosi liittyvät aiemman vamman liittyvät PRES., Vaikka PRES on yleensä täysin palautuva, se voi johtaa pysyvään loukkaantumiseen joissakin tilanteissa.
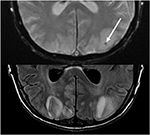
Kuva 10. Potilas, jolle on tehty takrolimuusin maksansiirto. T2 gradient recalled echo (top) osoittaa verenvuodon polttopisteen vasemman takaraivolohkon vasogeenisen turvotuksen sisällä. T2-FLAIR osoittaa enemmän tyypillinen toteamus liittyvät PRES signaalin poikkeavuus kahdenvälisissä takaraivo lohkoa.,
hoito
PRES-hoito pyritään tyypillisesti Pres-hoitoa aiheuttavan ensisijaisen etiologian (44) hallintaan. Esimerkiksi tapauksissa, kohonnut valtimoiden paineet, kohtelun tarkoituksena on korjata kohonnut veren paineet valvotussa ympäristössä, samanlainen lähestymistapa verenpainetautia kiireellisyyden/ hätä (45). Tyypillisesti, ei-nopea verenpaineen lasku on pyritty välttämään riskiä aiheuttaa iskeemisen aivojen taudin seurauksena rajuja verenpainetta alentava (46)., Joskus, kouristuslääkkeiden lääkkeitä käytetään yhdistelmähoitona, vaikka optimaalinen agentti(s), ajoitus, ja hoidon pituudesta edelleen kiistanalainen (4) (Kuva 11: Ennen ja Jälkeen).
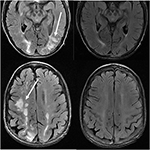
Kuva 11. Potilas, jolla on aiemmin ollut primaarinen myelofibroosi ja takrolimuusin luuydinsiirto. Aksiaalinen T2-FLAIR-kuvat osoittavat alueilla signaali poikkeavuus päälaen ja takaraivo lohkoa ja oikeassa otsalohkossa (vasen kuva)., Takrolimuusi lopetettiin ja seurantakuvat (oikeat kuvat) saatiin 6 viikkoa ensimmäisten kuvien jälkeen.
tapauksissa (ennalta)eklampsia, hoito on suunnattu oikea-aikainen toimitus sikiö sekä verenpaineen hallintaan ja magnesium sulfate for kohtauksen jälkeen (47). Asettaminen PRES aiheuttama kemoterapia-tai muu immunosuppressio aineet, kapeneva tai absoluuttinen lopettaminen lääke on osoittanut sekä kliinisten ja radiologisten parantaminen (48) (Kuva 12: Eklampsia)., Hypomagnesemia on PRESISSÄ yleinen löydös ja mahdollinen etiologinen tekijä. Siksi kirjoittajat ovat ehdottaneet, että magnesium täydentää voi olla hyödyllinen lisäosa PRES hallinta (49).
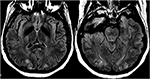
Kuva 12. Potilas, jolla on raskausmyrkytys ja kouristuskohtaus. Aksiaaliset T2-FLAIR-kuvat osoittavat symmetrisen signaalin poikkeavuuden molemminpuolisissa takaraivolohkoissa.,
Johtopäätös
PRES on ainutlaatuinen kokonaisuus, jonka ominaisuus kliinisiä ja neuroradiological havainnot, lisäksi lukemattomia hyvin dokumentoitu syitä. Vaikka tarkka pathophysiologic mekanismi(s) takana PRES ei ole vielä selvitetty (ja todellakin voi johtua yhdistelmä toisiinsa liittyviä prosesseja), yleisesti hyväksyttyihin mekanismi on toimintahäiriö veri-aivoesteen, mikä vasogenic turvotus taka-liikkeeseen ylivalta., Kuvantamisen ominaisuuksia ovat parhaiten arvioida neste-herkkä ARVOISA sekvenssit, joka paljastaa parieto-takaraivon hallitseva valkoinen asia T2 hyperintensities, vaikka monet epätyypillinen kuvantamisen ominaisuuksia voidaan nähdä, ja olisi pidettävä mielessä, kun arvioidaan haastavia tapauksia. Saatavilla on erilaisia kehittyneitä kuvantamisvälineitä, jotka auttavat vaikeissa tai epäselvissä tapauksissa. Hoidon tarkoituksena on hallita perussyytä kiinnittäen erityistä huomiota verenpaineen seurantaan ja mahdolliseen kohtausten estohoitoon.,
Kirjoittaja Maksut
eturistiriita
kirjoittajat ilmoittavat, että tutkimus on tehty ilman mitään kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdollisia eturistiriitoja.
1. Bartynski WS. Posteriorinen reversiibeli enkefalopatia-oireyhtymä, Osa 1: fundamentaalinen kuvantaminen ja kliiniset piirteet. Olen J Neuroradiol. (2008) 29:1036–42. doi: 10.3174 / ajnr.,A0928
CrossRef Full Text | Google Scholar
3. Bartynski WS. Posterior reversible encephalopathy syndrome, Part 2: controversies surrounding pathophysiology of vasogenic edema. Am J Neuroradiol. (2008) 29:1043–9. doi: 10.3174/ajnr.A0929
CrossRef Full Text | Google Scholar
5. Singer S, Grommes C, Reiner AS, Rosenblum MK, DeAngelis LM. Posterior reversible encephalopathy syndrome in patients with cancer., Oncologist. (2015) 20:806–11. doi: 10.1634/theoncologist.2014-0149
PubMed Abstract | CrossRef Full Text | Google Scholar
6. How J, Blattner M, Fowler S, Wang-Gillam A, Schindler SE. Chemotherapy-associated posterior reversible encephalopathy syndrome: a case report and review of the literature. Neurologist. (2016) 21:112–7. doi: 10.1097/NRL.,0000000000000105
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Habetz K, Ramakrishnaiah R, Raina SK, Fitzgerald RT, Hinduja A. Posterior reversible encephalopathy syndrome: a comparative study of pediatric versus adult patients. Pediatr Neurol. (2016) 65:45–51. doi: 10.1016/j.pediatrneurol.2016.09.001
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Fugate JE, Rabinstein AA., Posterior reversible encephalopathy syndrome: clinical and radiological manifestations, pathophysiology, and outstanding questions. Lancet Neurol. (2015) 14:914–25. doi: 10.1016/S1474-4422(15)00111-8
CrossRef Full Text | Google Scholar
9. Zama, D, Gasperini P, Berger M, Petris M, De Pasquale MD, et al. A survey on hematology-oncology pediatric AIEOP centres: the challenge of posterior reversible encephalopathy syndrome. Eur J Haematol. (2018) 100:75–82. doi: 10.1111/ejh.,12984
CrossRef Full Text | Google Scholar
12. Gupta V, Bhatia V, Khandelwal N, Singh P, Singhi P. Imaging findings in pediatric posterior reversible encephalopathy syndrome (PRES): 5 years of experience from a tertiary care center in India. J Child Neurol. (2016) 31:1166–73. doi: 10.1177/0883073816643409
PubMed Abstract | CrossRef Full Text | Google Scholar
13., Hinduja On, Habetz K, Raina S, Ramakrishnaiah R, Fitzgerald RT. Ennustavat huono tulos potilailla, joilla on posteriorinen palautuva enkefalopatia oireyhtymä. Int J Neurosci. (2017) 127:134–44. doi: 10.3109/00207454.2016.1152966
PubMed Abstrakti | CrossRef Koko Teksti | Google Scholar
15. MacKenzie ET, Strandgaard S, Graham DI, Jones JV, Harper AM, Farrar JK. Vaikutuksia akuutisti aiheuttama kohonnut verenpaine kissat pial valtimon kaliiperi, paikallinen aivojen verenkiertoa, ja veri-aivoesteen. Circ Res., (1976) 39:33–41. doi: 10.1161/01.RES.39.1.33
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Bartynski WS, Zeigler Z, Spearman MP, Lin L, Shadduck RK, Lister J. Etiology of cortical and white matter lesions in Cyclosporin-A and FK-506 neurotoxicity. Am J Neuroradiol. (2001) 22:1901–14.
PubMed Abstract | Google Scholar
21. Bartynski WS, Boardman JF, Zeigler ZR, Shadduck RK, Lister J., Posterior reversible encephalopathy syndrome in infection, sepsis, and shock. Am J Neuroradiol. (2006) 27:2179–90.
PubMed Abstract | Google Scholar
22. Mayama M, Uno K, Tano S, Yoshihara M, Ukai M, Kishigami Y, et al. Incidence of posterior reversible encephalopathy syndrome in eclamptic and patients with preeclampsia with neurologic symptoms. Am J Obstet Gynecol. (2016) 215:239.e1–e5. doi: 10.1016/j.ajog.2016.02.,039
PubMed Abstract | CrossRef Full Text | Google Scholar
23. McKinney AM, Short J, Truwit CL, McKinney ZJ, Kozak OS, SantaCruz KS, et al. Posterior reversible encephalopathy syndrome: incidence of atypical regions of involvement and imaging findings. Am J Roentgenol. (2007) 189:904–12. doi: 10.2214/AJR.07.2024
PubMed Abstract | CrossRef Full Text | Google Scholar
24., de Havenon A, Joos Z, Longenecker L, Shah L, Ansari S, Digre K. Posterior reversible encephalopathy syndrome with spinal cord involvement. Neurology. (2014) 83:2002–6. doi: 10.1212/WNL.0000000000001026
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Dandoy CE, Linscott LL, Davies SM, Leach JL, Myers KC, El-Bietar J, et al., Clinical utility of computed tomography and magnetic resonance imaging for diagnosis of posterior reversible encephalopathy syndrome after stem cell transplantation in children and adolescents. Biol Blood Marrow Transplant. (2015) 21:2028–32. doi: 10.1016/j.bbmt.2015.07.023
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Noda K, Fukae J, Fujishima K, Mori K, Urabe T, Hattori N, et al., Reversible cerebral vasoconstriction syndrome presenting as subarachnoid hemorrhage, reversible posterior leukoencephalopathy, and cerebral infarction. Intern Med. (2011) 50:1227–33. doi: 10.2169/internalmedicine.50.4812
CrossRef Full Text | Google Scholar
31. Doelken M, Lanz S, Rennert J, Alibek S, Richter G, Doerfler A, et al. Differentiation of cytotoxic and vasogenic edema in a patient with reversible posterior leukoencephalopathy syndrome using diffusion-weighted MRI. Diagn Interv Radiol., (2007) 13:125–8.
Google Scholar
32. Wartenberg KE, Parra A. CT and CT-perfusion findings of reversible leukoencephalopathy during triple-H therapy for symptomatic subarachnoid hemorrhage-related vasospasm. J Neuroimaging. (2006) 16:170–5. doi: 10.1111/j.1552-6569.2006.00031.x
CrossRef Full Text | Google Scholar
33. Vanacker P, Matias G, Hagmann P, Michel P., Cerebral hypoperfusion in posterior reversible encephalopathy syndrome is different from transient ischemic attack on CT perfusion. J Neuroimaging. (2015) 25:643–6. doi: 10.1111/jon.12158
CrossRef Full Text | Google Scholar
34. Lee SY, Kim SH, Lee SH, Baek HJ, Shon HS, Kim SS. Serial MR spectroscopy in relapsing reversible posterior leukoencephalopathy syndrome. Neurologist. (2009) 15:338–41. doi: 10.1097/NRL.,0b013e3181914af6
PubMed Abstract | CrossRef Full Text | Google Scholar
35. McKinney AM, Sarikaya B, Gustafson C, Truwit CL. Detection of microhemorrhage in posterior reversible encephalopathy syndrome using susceptibility-weighted imaging. Am J Neuroradiol. (2012) 33:896–903. doi: 10.3174/ajnr.A2886
PubMed Abstract | CrossRef Full Text | Google Scholar
38., Berger JR, Aksamit AJ, Clifford DB, Davis L, Koralnik IJ, Sejvar JJ, ym. PML diagnostiset kriteerit: KONSENSUSLAUSUMA AAN neuroinfectious disease-osiosta. Neurologia. (2013) 80:1430-8. doi: 10.1212 / VNL.0b013e31828c2fa1
PubMed Abstrakti | CrossRef Koko Teksti | Google Scholar
39. Aracki-Trenkić Ja Stojanov D, Trenkić M, Radovanovic Z, Ignjatovic J, Ristic S, et al., Atypical presentation of posterior reversible encephalopathy syndrome: clinical and radiological characteristics in eclamptic patients. Bosn J Basic Med Sci. (2016) 16:180–6. doi: 10.17305/bjbms.2016.1201
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Bartynski WS, Boardman JF. Distinct imaging patterns and lesion distribution in posterior reversible encephalopathy syndrome. Am J Neuroradiol. (2007) 28:1320–7. doi: 10.3174/ajnr.,A0549
PubMed Abstract | CrossRef Full Text | Google Scholar
46. Brickman AM, Reitz C, Luchsinger JA, Manly JJ, Schupf N, Muraskin J, et al. Long-term blood pressure fluctuation and cerebrovascular disease in an elderly cohort. Arch Neurol. (2010) 67:564–9. doi: 10.1001/archneurol.2010.70
PubMed Abstract | CrossRef Full Text | Google Scholar
47., Cozzolino M, Bianchi C, Mariani G, Marchi L, Fambrini M, Mecacci F. Therapy and differential diagnosis of posterior reversible encephalopathy syndrome (PRES) during pregnancy and postpartum. Arch Gynecol Obstet. (2015) 292:1217–23. doi: 10.1007/s00404-015-3800-4
PubMed Abstract | CrossRef Full Text | Google Scholar
48. Masetti R, Cordelli DM, Zama D, Vendemini F, Biagi C, Franzoni E, et al. PRES in children undergoing hematopoietic stem cell or solid organ transplantation. Pediatrics., (2015) 135:890–901. doi: 10.1542/peds.2014-2325
CrossRef Full Text | Google Scholar