13. huhtikuuta 2017, jonka NCI Henkilökunta
Brain scan lapsen kanssa DIPG kasvain, joka sijaitsee aivorungon.
Kaksi eri tutkimuksissa on havaittu potentiaalisia terapeuttisia tavoitteita käyttökelvottoman lasten aivokasvain, hajanainen luontainen pontine gliooma (DIPG). Näiden kohteiden estäminen tutkimuslääkkeillä hidasti kasvaimen kasvua DIPG: n eläinmalleissa.
aivorungossa sijaitseva kasvain on lähes tasaisesti kuolemaan johtava.,
”, Kuten lasten neurooncologist, se”s yksi kaikkein tuhoisia kasvaimia näemme,” sanoi Pratiti Bandopadhayay, M. B., B. S., Ph. D., Dana-Farber/Boston Children”s Syöpä ja Veren Häiriöt Keskus, joka oli ollut mukana tutkimuksissa. ”Meillä ei ole lainkaan parantavaa hoitoa näihin kasvaimiin.”
Vaikka suurin osa DIPG kasvaimia kuljettaa tietty geneettinen mutaatio, se oli aiemmin epäselvää, mikä rooli, jos mitään, mutantti proteiini pelaa kasvaimen kehitystä, ja onko sen toiminta voisi olla kohteena hoitoja.,
molemmissa uusissa tutkimuksissa tutkimusryhmät tutkivat ihmisen DIPG-solujen biologiaa tällä mutaatiolla ja tunnistivat ominaisuudet, jotka voivat altistaa ne hoidolle. Verrattuna ohjaus hoitoja, he huomasivat, huumeita kutsutaan PRC2 ja VETO-estäjät supistui DIPG kasvaimia hiiri malleja ja pidentyneet hiiret”s elämää.
molempien tutkimusten tuloksia, yksi tutkimusryhmä Northwestern University, ja toinen ryhmä, Kööpenhaminan Yliopisto, Tanska, julkaistiin 27. helmikuuta vuonna Nature Medicine.,
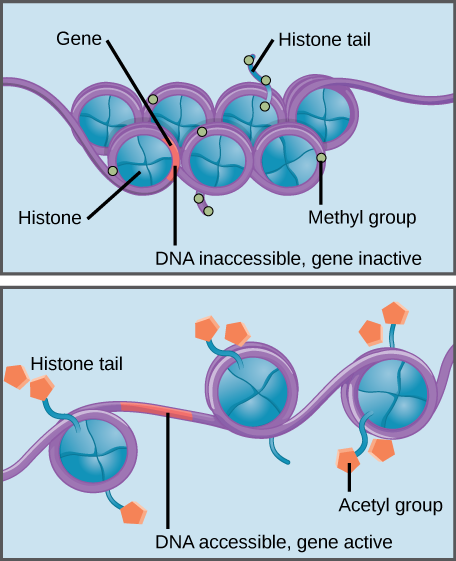
Histoni metylaatio vahvistaa histoni–DNA-vuorovaikutus, jolloin siihen liittyvät geenit saavuttamattomissa geenien ilmentyminen (aktiivinen). Histoniasetylaatio heikentää vuorovaikutusta, jolloin siihen liittyvät geenit ovat helposti saatavilla geenin ilmentymistä varten (aktiivinen).
Tunnistaminen Tavoite
Noin 5 vuotta sitten, tutkijat työskentelevät St., Jude-Washingtonin yliopiston Pediatric Cancer Genome Project-tutkimuksessa havaittiin, että lähes 80 prosentilla DPG-kasvaimista on histone H3-nimisen proteiinin geenissä erityinen mutaatio.
Että tällainen prosenttiosuus on suuri, kasvaimia on tämä sama mutaatio tuli yllätyksenä DIPG tutkimus yhteisö, sanoi Ali Shilatifard, Ph. D., ja Northwestern University Feinberg School of Medicine, johtaa tutkija yhdessä tutkimuksessa.
histonit ovat proteiiniperhe, joka auttaa paketoimaan DNA: ta kompakteihin rakenteisiin., Lyhyitä jaksoja DNA laskee noin histoni-proteiinien, kuten lanka kela, ja tuhansia DNA–kääritty histones (kutsutaan jaa twitteriinjaa) muodostavat kukin kromosomi.
spesifiset muutokset histoneihin voivat edistää tai estää geenien ilmentymistä. Esimerkiksi, kiinnitys kemiallisia yhdisteitä kutsutaan asetyyli ryhmien histones heikentää niiden vuorovaikutusta DNA: n kanssa, edistää geenien ilmentyminen. Toisaalta metyyliryhmien lisääminen histoneihin tekee DNA-tuulesta yleensä tiiviimpää histonien ympärillä estäen geenien ilmentymisen.,
Histoni H3-mutaation tunnistaminen DIPG-potilailla oli ensimmäinen askel, sanoi Tri Bandopadhay. ”Mutta voidaksesi hoitaa kasvaimia tuolla muutoksella sinun täytyy ymmärtää, mitä mutaatio tekee”, hän lisäsi.
aiemmassa tutkimuksessa tohtori Shilatifard kollegoineen käytti hedelmäkärpäsiä mutanttihistoroni H3-geenin toiminnan tutkimiseen. Verrattuna kärpäsiä, jotka oli normaali histoni H3 proteiineja, lentää mutantti versio oli enemmän histones, jotka olivat nastoitettu asetyyliryhmiä (asetyloitu)., Nämä asetyloidut histonit puolestaan sitoutuivat bromodomainipitoisiin (BRD) proteiineihin, jotka säätelevät geenien ilmentymistä.
– heidän nykyinen tutkimus, joka rahoitettiin osittain NCI, Luoteis tutkijat halusivat selvittää, onko mutant histoni oli sama funktio ihmisen soluissa. Todellakin, he huomasivat, että ihmisen paksusuolen syöpä tai munuaisten syöpä solujen muuttunut ilmaista mutatoitunut histoni H3 geeni oli enemmän asetyloitu histones kuin solut, jotka ilmaisivat normaali histoni H3 geeni.
ensimmäinen kirjoittaja, Andrea Piunti, filosofian tohtori.,, sitten tutkittu kaikki mutantti H3 histonit sijaitsevat koko genomit DPG kasvainsolujen kolme potilasta. Hänen analyysinsä paljasti, että monet mutanttihistorioita sisältävät nukleosomit asetyloituivat ja sitoutuivat BRD-proteiineihin.
lisäkokeet osoittivat, että BRD-proteiineilla voi olla suora rooli DIPG-kasvaimen kasvussa. Hoitoon ihmisen DIPG solujen tutkittavia lääkkeitä, jotka estävät BRD proteiineja, joita kutsutaan VETO-estäjät, hidastunut DIPG solujen kasvua verrattuna kontrollikäsittely., Ja tutkimuksissa hiirillä, joilla ihmisen DIPG solut istutetaan aivoihin varret, ne hoidettiin VETO-estäjien oli pienempiä kasvaimia ja elänyt kauemmin kuin hiirillä, joita hoidettiin ohjaus hoito.
Näiden kokeiden ”viittaavat siihen, että VETO-estäjät tarjoavat potentiaalinen terapeuttinen lähestymistapa DIPG”, sanoi Tohtori Shilatifard. Prekliiniset tutkimukset ovat osoittaneet, että useat eri syöpätyyppien—mukaan lukien leukemia ja glioblastooma—ovat myös herkkiä VETO-estäjät, hän lisäsi.,
Lisää Kohteeseen
Luoteis-ryhmä”s-analyysin ihmisen DIPG kasvain solujen mutantti histoni H3 paljasti myös, että lisäksi enemmän histoni H3 asetylointi, monet histones oli koristeltu metyyli-ryhmien (denaturoitu). Lisäksi he havaitsivat, että monien näiden histonien lähellä oli prc2—niminen entsyymi, joka liittää metyyliryhmiä Histoni H3—proteiineihin.
Nämä tulokset saivat tutkijat Northwestern tutkia PRC2 toimintaa., He havaitsivat, että prc2—aktiivisuuden estäminen—joko geneettisesti tai prc2-estäjällä nimeltä tazemetostat-vähensi DIPG-solujen kasvua.
”Yllättäen nämä tulokset osoittavat rooli PRC2 toiminto ylläpito DIPG kasvua,” Luoteis-ryhmä kirjoitti.
Kööpenhaminan ryhmä löysi myös todisteita, jotka tukivat PRC2: n roolia DIPG-kasvaimen kasvun edistämisessä. He havaitsivat, että tazemetostat ja toinen PRC2 estäjä vähensi kasvua hiiri aivosoluja tai ihmisen DIPG solujen mutantti histones, kun taas ohjaus hoito ei.,
Ja kun he laittoivat hiiren aivoissa solujen mutantti histones aivot normaalit hiiret tai hiirillä, jotka PRC2 oli geneettisesti tukossa, jotka puuttui PRC2 toimintaa elänyt kauemmin.
sen sijaan, kuitenkin, erillistä tutkimuksessa tutkimusryhmä Saksassa havaittiin, että solujen eri potilaiden kanssa DIPG eivät ole herkkiä tazemetostat, vaikka niiden kasvaimia oli histoni H3 mutaatio.
Askel Eteenpäin
Vuosikymmeniä kliiniset tutkimukset ovat osoittaneet, että DIPG kasvaimet ovat tunteettomia perinteiset kemoterapia, selitti Tohtori Bandopadhayay., Ja vaikka säteily voi lievittää oireita, se ei ole parantavaa, ja useimmat lapset, joilla on nestekaasu kuolee 2 vuoden kuluessa diagnoosista.
Vuonna 2015, kansainvälinen yhteenliittymä DIPG tutkijat porrastettuja yhdessä tutkia kaikki käytettävissä DIPG solun näytteitä. Heidän tutkimuksessa kävi ilmi, että DIPG solut kerättiin useista eri potilaat saivat surmansa histoni-muuttamalla huumeiden kutsutaan panobinostat (Farydak®). Panobinostaatti estää entsyymejä, jotka lisäävät asetyyliryhmiä histoneihin., Nyt tutkijat, jotka ovat osa NCI-tuettu Lasten Aivokasvain Konsortio, ovat testauksen turvallisuuden ja paras annos panobinostat lasten kanssa DIPG vaiheen I kliinisen tutkimuksen.
nyt molempien tutkimusten tulokset viittaavat mahdollisesti lupaaviin uusiin hoitostrategioihin, tohtori Shilatifard sanoi.
”haluamme siirtää VETO-estäjät osaksi faasi I-tutkimuksessa hoitoon DIPG, ja meidän kollegansa Ann & Robert H. Lurie Lasten”s Hospital of Chicago vievät eteenpäin ne tutkimukset,” hän sanoi.,
lisäksi useissa meneillään olevissa kliinisissä tutkimuksissa on tutkittu prc2: n estäjää TATSEMETOSTAATTIA sekä aikuisilla että lapsilla, joilla on erilaisia syöpiä. Mikään tämänhetkinen tutkimus ei kuitenkaan nimenomaan tutki TAZEMETOSTAATTIA lapsilla, joilla on nestekaasu.
On olemassa vielä monia avoimia kysymyksiä, sanoi Tohtori Bandopadhayay, mukaan lukien se, ovatko nämä tutkittavat lääkkeet on kyky ylittää veri–aivoesteen ja saavuttaa ihmisen aivot kasvaimia.
Dr., Bandopadhayy ja hänen kollegansa oppivat myös lisää DPG-biologiasta tutkimalla koepaloista saatuja kasvainsoluja ruumiinavauksista saatujen lisäksi. Saada biopsia näytteitä on ollut mahdollista vasta viime aikoina suuria parannuksia neurokirurgisten tekniikoita, hän selitti.
”It”s an exciting time”, hän sanoi. ”Siellä” on paljon työtä käynnissä juuri nyt. Perimmäinen tavoite on pystyä hoitamaan näitä lapsia niin, että heillä on mahdollisuus parantaa minimaalinen sivuvaikutuksia.”