April13,2017 년에 의하여,NCI 직원
뇌 검사와 아이의 DIPG 종양,에 위치한 뇌.
두 가지 별도의 연구가 확인되는 잠재적인 치료 대상에서 작동하지 않는 소아과 뇌종양 확산유 pontine 신경(DIPG). 조사 약물로 이러한 표적을 차단하면 DIPG 의 동물 모델에서 종양 성장이 느려졌습니다.뇌 줄기에 위치한 종양 인 DIPG 는 거의 균일하게 치명적입니다.,
“소아 neurooncologist,그것은”하나의 가장 파괴적인 종양을 우리가 볼 수,”고 말했다 Pratiti Bandopadhayay,M.B.B.S.,Ph.D.,의 다나-파버/는 보스턴 어린이”s 암과 혈액 장애 센터,누구인지에 관련된 학문. “우리는이 종양에 대한 치료 적 치료법이 전혀 없다.”
는 동안 대부분의 DIPG 종양을 수행한 특정 유전자 돌연변이,그것은 이전에 불명확하 어떤 역할 경우,돌연변이 단백질이 놀이에 종양을 개발하는지 여부,그 기능을 대상으로 수여 있습니다.,
모두 새로운 학문에,연구 팀은 조사서 생물학의 인간 DIPG 세포 이 돌연변이와적 특성을 식별할 수 있는 그들을 만들에 취약한 치료입니다. 제어와 비교 트리트먼트,그들을 발견,약물로 알려진 PRC2 및 베팅을 억제제 shrank DIPG 종양에서 마우스 모델과 길게 쥐”s lives.
Northwestern University 의 연구 그룹과 덴마크의 코펜하겐 대학(University Of Copenhagen)그룹의 두 연구 결과는 2 월 27 일 Nature Medicine 에 발표되었습니다.,
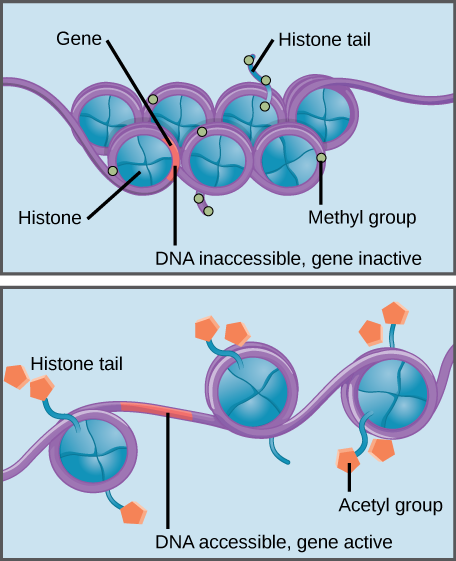
히스톤 메틸화를 강화하고 히스톤–DNA interaction,기 관련 유전자에 액세스하는 유전자 발현(비활성 상태). 히스톤 아세틸 화는 상호 작용을 약화시켜 관련 유전자가 유전자 발현에 접근 할 수있게한다(활성).
를 식별하는 대상
정가 5 년 전에 연구자들은 작업에서트, Jude-Washington University Pediatric Cancer Genome Project 는 DIPG 종양의 거의 80%가 histone H3 이라는 단백질에 대한 유전자의 특정 돌연변이를 가지고 있음을 발견했습니다.
는 높은 백분율의 종양이 같은 돌연변이 놀라게 했의 DIPG 연구 커뮤니티,알리 Shilatifard,Ph.D.,의 노스웨스턴 대학교 feinberg 의학의 지도자 중 하나에 대한 연구이다.
히스톤은 DNA 를 컴팩트 한 구조로 패키징하는 데 도움이되는 단백질 계열입니다., 짧은 섹션의 DNA 바람에게 히스톤 단백질과 같은 스레드에 스풀,그리고 수천의 DNA–감 히스톤(라 nucleosomes)각 염색체입니다.
히스톤에 대한 특이 적 변형은 유전자 발현을 촉진 시키거나 예방할 수있다. 예를 들면,첨부 파일이라고 부르는 화합물의 아세틸 그룹 히스톤 약화의 상호 작용과 함께 DNA 를 추진,유전자 발현. 반면에,히스톤에 메틸 그룹을 첨가하면 일반적으로 DNA 가 히스톤 주위에서 더 단단히 감겨져 유전자 발현을 방지합니다.,
DIPG 환자에서 히스톤 H3 돌연변이의 존재를 확인하는 것이 첫 번째 단계라고 Bandopadhayay 박사는 말했다. “그러나 그 변화로 종양을 치료할 수 있으려면 돌연변이가 무엇을하고 있는지 이해해야한다”고 덧붙였다.
이전 연구에서 Shilatifard 박사와 그의 동료들은 과일 파리를 사용하여 돌연변이 히스톤 H3 유전자의 기능을 연구했습니다. 비교와 파리는 일반적인 H3 히스톤 단백질은,파리로 돌연변이 버전했다 더 히스톤 있던 박진 아세틸 그룹(acetylated)., 차례로,이들 아세틸 화 된 히스톤은 브로 모도 메인 함유(BRD)단백질이라고 불리는 분자에 의해 결합되어 유전자 발현을 조절한다.
에 대한 현재 연구에 의해 부분적으로 자금을 지원한 구상흑연주철,노스웨스턴 연구원은 원하는지 여부를 확인 돌연변이 히스톤 같은 함수는 인간의 세포에서. 실제로,그들은 인간의 대장암 또는 신장 암세포 변경을 표현하는 돌연변이 histone H3gene 했다 더 아세틸화 히스톤상세포로 표현하는 정상적인 histone H3gene.
첫 번째 저자,Andrea Piunti,Ph.D., 그런 다음 3 명의 환자에서 DIPG 종양 세포의 게놈 전체에 위치한 모든 돌연변이 H3 히스톤을 검사했습니다. 그의 분석에 따르면 돌연변이 히스톤을 함유 한 많은 뉴 클레오 솜이 아세틸 화되어 BRD 단백질에 결합되어 있음이 밝혀졌습니다.
추가 실험은 BRD 단백질이 DIPG 종양 성장에 직접적인 역할을 할 수 있음을 보여 주었다. BET 억제제라고 불리는 BRD 단백질을 차단하는 조사 약물로 인간 DIPG 세포를 치료하면 대조군 치료와 비교하여 DIPG 세포 성장이 느려졌다., 과 연구에서는 쥐의 인 DIPG 세포를 이식으로 자신의 두뇌 줄기,그 처리과 내기를 억제제했던 작은 종양하고보다 더 오래 살았 마우스로 처리 제어 치료입니다.
이러한 실험은”BET 억제제가 DIPG 에 대한 잠재적 인 치료 접근법을 제공한다는 것을 시사한다”고 Shilatifard 박사는 말했다. 전임상 연구에 따르면 백혈병과 아교 모세포종을 포함한 여러 가지 다른 암 유형도 내기 억제제에 민감하다고 그는 덧붙였다.,
추가로 대상
노스웨스턴 그룹”s 분석의 인간 DIPG 종양 세포로 돌연변이 histone H3 도 공개하는 외에 더 histone H3acetylation,많은 히스톤었으로 장식 메틸(메틸화). 또한,그들이 발견되는 라는 효소 PRC2—붙이는 메틸 그룹 히스톤 H3 단백질—현재 근처의 많은 이들 히스톤.
이러한 결과는 Northwestern 연구원들이 PRC2 활동에 대해 더 자세히 조사하도록 자극했습니다., 그들이 발견되는 차단 PRC2 활동거나 유전자 변형 또는 PRC2 억제물이라고 tazemetostat—감 DIPG 세포 성장이다.
“예기치 않게,이러한 결과를 보여주는 역할을 PRC2 기능의 유지에 DIPG 성장은”노스 웨스턴 그룹을 썼다.
코펜하겐 그룹은 또한 DIPG 종양 성장을 촉진시키는 PRC2 의 역할을 뒷받침하는 증거를 발견했다. 그들은 관찰되는 tazemetostat 및 다른 PRC2 억제물 감소의 성장을 쥐의 뇌 세포가 또는 인 DIPG 세포로 돌연변이 히스톤는 반면,제어를 처리하지 않았다.,
때와 그 이식 쥐의 뇌 세포와 돌연변이 히스톤으로 두뇌의 정상적인 쥐거나 쥐에서는 PRC2 유전으로 차단되는 사람들이 부족 PRC2 활동이 더 이상 살고.
대조적으로,그러나,별도의 연구에 의해 연구 그룹은 독일에서 발견되는 세포에서 다른 환자 DIPG 들에 민감하지 않 tazemetostat,비록 그들의 종양이 있었 histone H3 돌연변이.
앞으로 단계
수십 년의 임상 시험는 다음과 같 DIPG 종양이를 구분하는 전통적 화학요법,설명한 박사 Bandopadhayay., 그리고 방사선이 증상을 완화시킬 수는 있지만 치료법이 아니며 DIPG 를 가진 대부분의 어린이는 진단 후 2 년 이내에 사망합니다.
에서 2015,국제 컨소시엄의 DIPG 연구팀은 줄무늬를 연구하기 위해 함께 사용할 수 있는 모든 DIPG 셀 샘플입니다. 자신의 학문을 밝혔 DIPG 세포에서 수집한 여러 가지 환자에 의해 살해당한 히스톤-수정하는 약물이라고 panobinostat(Farydak®). Panobinostat 은 아세틸 그룹을 히스톤에 추가하는 효소를 차단합니다., 지금 하는 연구자의 일부는 NCI-지원되는 소아과 뇌종양 컨소시엄,테스트의 안전성과 최고의 용량의 panobinostat 에 대한 아이들과 함께 DIPG 에서 단계 I 임상 시험입니다.
이제 두 연구의 결과는 잠재적으로 유망한 새로운 치료 전략을 지적한다고 Shilatifard 박사는 말했다.
“우리가 이동하려는 내기를 억제제로 phase I 연구에 대한 치료의 DIPG,그리고 우리의 동료들에 앤&Robert H.Lurie 어린이”s 병원 시카고 앞으로 밀고 사람들과 연구,”고 말했다.,
또한,여러 가지 지속적인 임상 연구 테스트 tazemetostat,the PRC2 억제제 모두에서 성인과 소아환자와 함께 다양한 암입니다. 그러나 dipg 를 가진 어린이의 tazemetostat 을 구체적으로 조사하는 현재의 연구는 없습니다.
아직도 많은 답이 없는 질문에,박사는 말했 Bandopadhayay 지 여부를 포함하여 이러한 임상하는 능력이 있는 십자가의 뇌혈관 및 reach 인간의 뇌에 종양이다.
박사., Bandopadhayay 와 그녀의 동료들도 배에 대해 더 DIPG 생물학을 공부해서 종양 세포에서 얻은 생체검사,그 외에도에서 얻은 부검. 생검 샘플을 얻는 것은 신경 외과 기술의 주요 개선으로 최근에야 가능 해졌다 고 그녀는 설명했다.”그것은 흥미 진진한 시간”이라고 그녀는 말했다. “거기”는 지금 진행중인 많은 작업입니다. 궁극적 인 목표는 최소한의 부작용으로 치료할 수있는 기회를 갖도록이 아이들을 치료할 수있게하는 것입니다.”