Innledning
Posterior reversibel encefalopati syndrom (PRES), først beskrevet av Hinchey et al. i 1996, representerer en nevrologisk lidelse med variert klinisk presentasjon og typisk imaging funn av parieto-occipital dominerende mønster av vasogenic ødem (1, 2). Det er mange dokumenterte årsaker til PRES, med tilfeller først beskrevet i innstillingen av forhøyet arteriell press., Eksempler på kliniske situasjoner der PRES kan sees inkluderer: hypertensiv krise, (pre)eclampsia, nyresykdom, autoimmune sykdommer, og cytotoksiske medikamenter, blant annet (3, 4) (Tabell 1). PRES kan oppstå i alle aldersgrupper og har en høyere forekomst pris i kvinnelige pasienter (7, 8). Selv om dagens litteratur er relativt spredt i forhold til voksne bestander, særlig nevnes av PRES i pediatrisk pasient., Pediatriske pasienter har en lignende kliniske presentasjonen som den voksne befolkningen, med hypertensjon, beslag, og endret mental status blir felles sykdom manifestasjoner (9). Til tross for de fleste tilfeller av pediatric PRES blir rapportert i onkologi pasienter, særlig den post-stem-cellen transplantasjon pasienter (10, 11), en studie av Gupta et al. (12) fant at nyresykdom var kanskje den vanligste årsaken til PRES i pediatrisk pasient. I sin studie, pediatriske pasienter hadde en tendens til å ha mer atypisk imaging funn (62.5%), inkludert frontallappen engasjement (56%).,
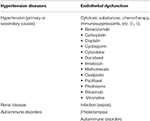
Tabell 1. Store sykdom stater forbundet med PRES.
Kliniske manifestasjoner som er til akutt subakutt og spenner fra hodepine og synsforstyrrelser til endrede nivåer av bevissthet og beslag i mer alvorlige tilfeller (1). Behandling er vanligvis rettet mot målretting den underliggende årsaken, med vanligvis reversible symptomer og bildebehandling funnene i de fleste tilfeller (8)., Selv om resultatene er generelt gunstig med riktig ledelse, dårlig kliniske resultatene har vært assosiert med pre-eksisterende diabetes mellitus, og involvering av corpus callosum, men andre pålitelige imaging biomarkører for prognostication er per i dag mangler (13). Neuroradiological imaging spiller en fundamental rolle i diagnostisering av PRES med den typiske bildebehandling funksjoner beste verdsatt på magnetisk resonans imaging (MRI) (2).
Pathophysiology
nøyaktig pathophysiologic mekanismen(e) bak PRES har ennå ikke blitt fullt ut belyst og er fortsatt kontroversielt (3)., Det er for tiden to større foreslåtte mekanismer for pathophysiology av PRES (Figur 1). Den første teorien foreslår økt arteriell presset som den primære faktor (8). Rask stiger i blodet presset til slutt overvinne autoregulatory evner av cerebral vaskulatur forårsaker vaskulær lekkasje og resulterende vasogenic ødem (14). Det er endelige blod-hjerne-barrieren (BBB) dysfunksjon med proteiner som passerer gjennom de trange-krysset (15)., Områdene er levert av bakre kretsløp (vertebrale arteriene, basilar arterien, og arteria cerebri posterior) er eksepsjonelle risiko i forhold til den fremre kretsløp (interne carotis, midt cerebrale arterier, og fremre cerebrale arterier) på grunn av mangel av sympatiske tone av basilar arterien blodkarene (8)., En beslektet teori foreslått av noen postulerer at ekstreme hypertensjon resultater i vasospasm og lokal iskemi som fører til BBB sammenbrudd og resulterende vasogenic ødem, som ble observert hos pasienter som behandles med immundempende midler ciklosporin A og FK-506 (16). Avbrudd i BBB fører til at den typiske funn av vasogenic ødem vs. cytotoksiske ødem (som kan sees i innstillingen av akutt infarkt og representerer økt intracellulære vanninnhold på grunn av tap av den vanlige osmotisk gradient i innstillingen av celledød (17).,
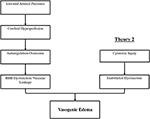
Figur 1. To store teorier av pathophysiology av PRES. Teori 1 er den hypertensive og cerebral hyperperfusion teori og Teori 2 er endotelial dysfunksjon teori.
Den andre store teori omhandler det faktum at opp til 30% av pasienter med PRES ikke viser forhøyet arteriell presset som er nødvendig for å overskride autoregulatory kontroll av cerebral vaskulatur (18, 19)., Denne teorien foreslår at endotelial dysfunksjon er den primære årsaken, som kan være forårsaket av ulike endogene eller eksogene toksiner (20). Denne teorien kan forklare funnene av PRES sett hos pasienter som får immunsuppressiv medisiner og/eller kjemoterapi, og også pasienter med sepsis (21, 22). I denne modellen, som sirkulerer giftstoffer føre til vaskulær skade med påfølgende utvikling av vasogenic ødem. Endothelial skade fører til ytterligere utslipp av vasoconstrictive og immunogenic agenter, som kan føre til vasospasm og/eller økt vaskulær permeabilitet., Til slutt, endotelial dysfunksjon slik at for vaskulær lekkasje og vasogenic ødem er den drivende faktoren bak PRES, uavhengig av den primære cerebral vaskulatur unormalt (i tilfelle av arteriell hypertensjon) eller sekundært til sirkulerer giftstoffer. En oppsummering av disse to teoriene, så vel som en liste av tidligere rapporterte chemotherapeutics og andre immunsuppressive er vist i Figur 2.
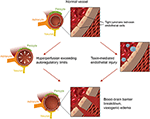
Figur 2. Illustrasjon av de to store teorier om den underliggende pathophysiology av PRES., Anerkjennelse: Gjengitt med tillatelse av Caroline O ‘ Driscoll, MA (Hun illustrerte dette på sin egen og er ansatt i vår university).
Kliniske manifestasjoner, avhenger av de involverte regionen(s) av hjernen, og dermed presentasjon kan være bred. For eksempel, primær involvering av occipital lobes kan resultere i visuelle forstyrrelser/hallusinasjoner. Fokale nevrologiske underskudd tilsvarende plasseringen av fokale lesjoner oppstår i ~5-15% av pasienter med PRES (23)., Sjelden, ryggmargen engasjement kan resultere i kliniske tegn og symptomer av myelopati eller lammelse (24).
Imaging
Som navnet antyder, PRES vanligvis manifesterer seg på bildebehandling studier som posterior-dominerende hvit materie vasogenic ødem. Parietal og occipital lobes er nesten universelt involvert, og funnene er vanligvis symmetriske og bilaterale (1). Involvering av frontallappene, spesielt i tilknytning til superior frontal sulci, er også ofte sett., Vasogenic ødem, selv om det kan innebære cerebral grå materie, er ofte lettere verdsatt i subkortikale hvit materie. CT-undersøkelse er ofte den første avbildning test i innstillingen av akutte nevrologiske symptomer og kan demonstrere hvit materie hypoattenuation i berørte regioner (25) (Figur 3: CT av PRES). Samlet sett er funnene er best avbildet av MR som viser økt følsomhet og bedre anatomiske karakterisering i forhold til CT (26). I tillegg, MR kan bidra til å skille andre patologiske tilstander som kan ha klinisk tilsvarende for å PRES., På T2-vektede og T2 FLAIR (væske-svekket inversion recovery) sekvenser, i særdeleshet, er mest nyttig for å oppdage vasogenic ødem på MR (Figur 4: MR av PRES; Figur 5: MR av PRES Koronal).
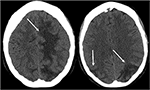
Figur 3. Pasienter med systemisk lupus erythematosus og hurtig progredierende glomerulonefritt presentere med anfall. Ikke-kontrast CT-bilder av hodet viser vasogenic ødem i bilaterale parietal-og occipital lobes, venstre større enn høyre, samt forlengelse til venstre frontallappen.,
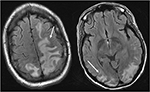
Figur 4. Pasienter med systemisk lupus erythematosus og hurtig progredierende glomerulonefritt presentere med anfall. T2-STIL bilder av hodet viser vasogenic ødem i bilaterale parietal-og occipital lobes, venstre større enn høyre, samt forlengelse til venstre frontallappen. Merk at vasogenic mønster av ødem, det er sparsom av signal abnormitet i cortex.
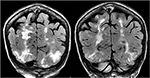
Figur 5., Pasienter med en historie med primær myelofibrose og bein marg transplantasjon på Takrolimus presentere med første gang anfall. Koronal T2-STIL sekvenser viser omfattende signal abnormitet i de bilaterale occipital og parietal-kammer, som er typisk med PRES.
differensialdiagnose for PRES er bred og omfatter selskaper med lignende confluent T2 hvit materie hyperintensity., Her er noen eksempler: iskemi/infarction (spesielt bakre kretsløp), demyeliniserende sykdommer, smittsomme etiologies (meningitt, encefalitt), progressiv multifokal leukoencefalopati (PML), vaskulitt, og ulike metabolske forstyrrelser (27). En klinisk relatert entitet kalt reversible cerebral vasoconstriction syndrom (RCVS) er antatt å være forårsaket av endringer i cerebral vaskulær tone resulterer i vasoconstriction., RCVS manifesterer seg som tilbakevendende tordenbrak hodepine, anfall, hjerneslag, og ikke-aneurysmal subarachnoid blødning (28), som kan forveksles med PRES på klinisk grunnlag. Denne enheten oppstår vanligvis i den post-partum perioden eller etter eksponering for adrenerge eller serotonerge medisiner. RCVS kan vanligvis diagnostiseres med angiografiske undersøkelser viser multifokal områder av innsnevring involverer cerebrale arterier (29). Denne diagnosen kan forveksles med det faktum at RCVS og PRES ofte forekommer samtidig, som neuroradiologist bør være oppmerksom på for å unngå misdiagnosis (30).,
PRES kan vanligvis skilles fra akutt iskemi fordi sistnevnte alltid viser cytotoksiske ødem og spredning begrensning. Begrenset spredning i akutt iskemi kan være lett funnet på diffusjon-vektet imaging (DWI) og tilsynelatende tilfeldig koeffisient (ADC) som en hyperintense signal på DWI med tilsvarende redusert signal på ADC (på grunn av den relativt redusert bevegelse av intracellulære vann molekyler)., Vasogenic ødem i innstillingen av PRÉS, på den annen side, kan vise hyperintense signal på DWI som ikke er ledsaget av en tilsvarende redusert signal på ADC (31). I tillegg, akutt iskemi har en tendens til å være ensidig og innen en enestående vaskulær territorium. Mens vurdering for spredning begrensning for å skille PRES fra iskemisk unormalt generelt er pålitelig, det er sjeldne tilfeller av PRES som kan være forbundet med områder av diffusjon begrensning lagt på områder av mer klassisk sett isolert vasogenic ødem.,
«Avansert» imaging teknikker i PRES har nylig blitt beskrevet som et supplement verktøy i vanskelige eller tvetydige saker. Disse advanced imaging teknikker inkluderer: CT/MR-perfusjon, MR-Spektroskopi (MRS), Mottakelighet vektet imaging (SWI), og nukleærmedisin teknikker, inkludert single-foton emisjon tomografi (SPECT) og positron emisjon tomografi (PET) med varierende radiotracers. Selv om en full diskusjon er utenfor omfanget av denne gjennomgangen, et utvalg av bildebehandling funn kan bli sett på disse avanserte teknikker til å foreslå en diagnose av PRES., Hyperperfusion kan bli sett på CT/MR-perfusjon studier har vist ved økt cerebral blodstrøm og blod volum med redusert tid til perfusjon og mener transitt tid (32) selv om tilfeller av hypoperfusion har blitt rapportert (33). På MRS, det er generelt en reduksjon i N-Acetylaspartate (NAA)/Kreatin (Cr) og NAA/Kolin (Chol) forhold, tyder på en forstyrrelse av normal synapser og neuroaxonal funksjon (34). SWI kan bidra til å identifisere tilstedeværelsen av blødning i PRES, med høyere følsomhet enn GRE imaging (35)., SPECT/PET imaging vanligvis viser enten hyperperfusion eller hypoperfusion (tilsvarende CT/MR-perfusjon studier) med lav metabolisme av FDG-PET (36).
i Tillegg, PRES kan skilles fra andre forhold, for eksempel autoimmune encefalitt i innstillingen av akutt disseminert encefalomyelitt (ADEM) av den tidligere»s diffuse bilaterale men asymmetriske vasogenic ødem (37)., PML kan ha et likt utseende i forhold til PRES, ha en parieto-occipital overvekt, men kan være preget av sin mer ensidig eller asymmetrisk engasjement, samt forkjærlighet for subkortikale hvit materie (38).
Atypisk Bildebehandling Funksjoner
Atypisk funksjoner av PRES inkluderer områdene i kontrast ekstrautstyr, blødning eller spredning restriksjon (39)., Selv om parietal og occipital lobes er vanligvis involvert, atypisk områder av engasjement kan bli sett, inkludert: hjernestammen, lillehjernen, corpus callosum, og andre cerebral områder, med mer fellesområder inkludert frontallappene (sett i opp til 68%) og dårligere tinninglappene (opptil 40%) (23, 40) (Figur 6: Cerebellum; Figur 7: Hjernestammen).
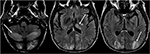
Figur 6. Pasienter med lever-transplantasjon 6 uker tidligere. Pasienten ble startet på Takrolimus etter levertransplantasjon., T2-STIL bilder av hjernen viser signal abnormitet i occipital lobes. Det er også omfattende signal unormalt sett i bilaterale lillehjernen hjernehalvdel, og i thalami. Disse funnene raskt løst etter avsluttet Tacrolimus.
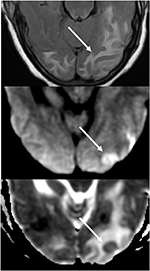
Figur 7. Pasienter med ukontrollert hypertensjon presentere med endring i mental status. T2-STIL (øverst) bildet viser ødem i occipital lobes., DWI (midten) og ADC-kart (nederst) bildene viser en liten pil av begrenset spredning, med hyperintense signal på DWI og tilsvarende hypointensity på ADC kartet.
i Tillegg et tidlig funn av PRES, som kan gå forut for den typiske parieto-occipital ødem inkluderer mild sulcal TEFT hyperintensity og leptomeningeal ekstrautstyr på post-kontrast T1-vektede bilder, som beskrevet av Nakagawa et al. (41). Benziada-Boudour et al., (42) beskrevet en løpende utvikling av cytotoksiske ødem, resulterende i en begrenset spredning (Figur 8: Diffusjon Begrensning). Iboende i navnet på sykdommen prosessen, de funn som er relatert til PRES er vanligvis reversible, med normalisering av kliniske og bildebehandling funn når det provoserende spørsmålet er behandlet. Imidlertid, i noen tilfeller, områder med begrenset spredning kan til slutt resultere i varig skade på hjernen parenchyma (Figur 9: Laminær Nekrose)., Blødning er mindre vanligvis sett i PRES, som forekommer i 5-30% av tilfellene, men bør bli anerkjent som å ikke tro at dette for å finne en annen patologisk enhet i den aktuelle kliniske setting av PRES (39). Imaging funn i blødning kan omfatte: focal hematom, petechial gyral blødning, og/eller subarachnoid blødning (43) (Figur 10: Blødning).
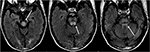
Figur 8. Pasienter med en historie med levertransplantasjon to uker tidligere på Tacrolimus., T2-STIL bilder som viser signal abnormitet i mellomhjernen, pons, og overlegen lillehjernen peduncles.
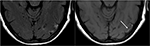
Figur 9. T2-STIL (til venstre) bildet av en pasient med ukontrollert hypertensjon og før imaging indikerer PRES (se Figur 6), som nå kontrolleres og 6 uker senere, viser oppløsningen av det tidligere sett ødem. Små områder av gliosis på grunn av skade er sett i venstre tinninglapp. Axial ikke-kontrast T1 viser kurvelineære kortikale laminær nekrose knyttet til tidligere skade i slekt å PRES., Mens PRES generelt er fullt reversibel, kan det føre til permanent skade i noen situasjoner.
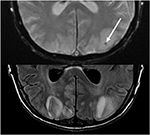
Figur 10. Pasient med en tidligere levertransplantasjon på Tacrolimus. T2 gradient fortalte echo (øverst) viser et satsingsområde, og av blødning i vasogenic ødem i venstre occipital lobe. T2-STIL viser mer typisk å finne i slekt å PRES med signal abnormitet i de bilaterale occipital lobes.,
Behandling
Behandling av PRES er vanligvis rettet mot å kontrollere den primære etiologi forårsaker PRES (44). For eksempel, i tilfeller av forhøyede arterielle trykket, behandling er rettet mot utbedring av forhøyet blod press i et kontrollert miljø, lik tilnærming for hypertensive haster/ emergency (45). Vanligvis, et ikke-rask reduksjon i blodtrykk er søkt å unngå risikoen for å forårsake iskemisk cerebral sykdom som et resultat av drastiske blodtrykkssenkende (46)., Noen ganger, krampestillende medikamenter brukes som supplement terapi, selv om den optimale agent(s), tidspunkt og varighet av behandling er fortsatt kontroversielt (4) (Figur 11: Før og Etter).
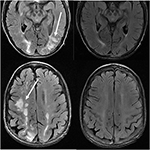
Figur 11. Pasienter med en historie med primær myelofibrose og bein marg transplantasjon på Tacrolimus. Axial T2-STIL bilder som viser de områdene av signal abnormitet i parietal-og occipital lobes, og høyre frontal lobe (venstre bilder)., Den Tacrolimus ble stoppet og følge opp bilder (høyre bilde) ble innhentet 6 uker etter den første bildene.
I tilfelle av (pre)eclampsia, behandling er rettet mot rettidig levering av fosteret, samt blodtrykk ledelse og magnesium sulfat for beslag profylakse (47). I innstillingen av PRES indusert av kjemoterapeutiske eller andre immunsuppresjon agenter, nedtrapping eller absolutt seponering av medikamentet har vist både kliniske og radiologiske forbedring (48) (Figur 12: Eclampsia)., Hypomagnesemia er et vanlig funn i PRES og mulige etiologiske faktorer. Derfor, forfattere har foreslått at magnesium tilskudd kan være et nyttig supplement i PRES management (49).
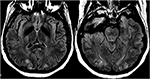
Figur 12. Pasient med eclampsia og presentere med anfall. Axial T2-STIL bilder som viser symmetrisk signal abnormitet i de bilaterale occipital lobes.,
Konklusjon
PRES er en unik enhet med karakteristiske kliniske og neuroradiological funn, i tillegg til utallige godt dokumentert årsaker. Selv om den eksakte pathophysiologic mekanismen(e) bak PRES og har ennå til å bli belyst (og faktisk kan være på grunn av en kombinasjon av beslektede prosesser), generelt akseptert mekanisme er dysfunksjon av blod-hjerne-barrieren som resulterer i vasogenic ødem med posterior-sirkulasjon overvekt., Bildebehandling funksjoner er best evaluert på væske-sensitive MR-sekvenser som avslører parieto-occipital dominerende hvit materie T2 hyperintensities, selv om mange atypisk bildebehandling funksjoner kan bli sett og bør holdes i bakhodet når du vurderer utfordrende saker. Ulike avansert bildebehandling verktøy er tilgjengelig for å hjelpe i vanskelige eller tvetydige saker. Behandlingen er rettet mot å behandle den underliggende årsaken med spesiell oppmerksomhet for å blodtrykk overvåking og mulig beslag profylakse.,
Forfatter Bidrag
interessekonflikt
forfatterne erklærer at forskningen ble utført i fravær av kommersielle eller finansielle forhold som kan oppfattes som en potensiell interessekonflikt.
1. Bartynski WS. Posterior reversibel encefalopati syndrom, Del 1: grunnleggende bildebehandling og kliniske funksjoner. Am J Neuroradiol. (2008) 29:1036-42. doi: 10.3174/ajnr.,A0928
CrossRef Full Text | Google Scholar
3. Bartynski WS. Posterior reversible encephalopathy syndrome, Part 2: controversies surrounding pathophysiology of vasogenic edema. Am J Neuroradiol. (2008) 29:1043–9. doi: 10.3174/ajnr.A0929
CrossRef Full Text | Google Scholar
5. Singer S, Grommes C, Reiner AS, Rosenblum MK, DeAngelis LM. Posterior reversible encephalopathy syndrome in patients with cancer., Oncologist. (2015) 20:806–11. doi: 10.1634/theoncologist.2014-0149
PubMed Abstract | CrossRef Full Text | Google Scholar
6. How J, Blattner M, Fowler S, Wang-Gillam A, Schindler SE. Chemotherapy-associated posterior reversible encephalopathy syndrome: a case report and review of the literature. Neurologist. (2016) 21:112–7. doi: 10.1097/NRL.,0000000000000105
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Habetz K, Ramakrishnaiah R, Raina SK, Fitzgerald RT, Hinduja A. Posterior reversible encephalopathy syndrome: a comparative study of pediatric versus adult patients. Pediatr Neurol. (2016) 65:45–51. doi: 10.1016/j.pediatrneurol.2016.09.001
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Fugate JE, Rabinstein AA., Posterior reversible encephalopathy syndrome: clinical and radiological manifestations, pathophysiology, and outstanding questions. Lancet Neurol. (2015) 14:914–25. doi: 10.1016/S1474-4422(15)00111-8
CrossRef Full Text | Google Scholar
9. Zama, D, Gasperini P, Berger M, Petris M, De Pasquale MD, et al. A survey on hematology-oncology pediatric AIEOP centres: the challenge of posterior reversible encephalopathy syndrome. Eur J Haematol. (2018) 100:75–82. doi: 10.1111/ejh.,12984
CrossRef Full Text | Google Scholar
12. Gupta V, Bhatia V, Khandelwal N, Singh P, Singhi P. Imaging findings in pediatric posterior reversible encephalopathy syndrome (PRES): 5 years of experience from a tertiary care center in India. J Child Neurol. (2016) 31:1166–73. doi: 10.1177/0883073816643409
PubMed Abstract | CrossRef Full Text | Google Scholar
13., Hinduja En, Habetz K, Raina S, Ramakrishnaiah R, Fitzgerald RT. Prediktorer for dårlig utfall hos pasienter med posterior reversibel encefalopati syndrom. Int J Neurosci. (2017) 127:134-44. doi: 10.3109/00207454.2016.1152966
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
15. MacKenzie ET, Strandgaard S, Graham DI, Jones JV, Harper ‘ AM, Farrar JK. Virkninger av akutt indusert hypertensjon i katter på pial arteriolar kaliber, lokale cerebral blodstrøm, og blod-hjerne barrieren. Circ Res., (1976) 39:33–41. doi: 10.1161/01.RES.39.1.33
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Bartynski WS, Zeigler Z, Spearman MP, Lin L, Shadduck RK, Lister J. Etiology of cortical and white matter lesions in Cyclosporin-A and FK-506 neurotoxicity. Am J Neuroradiol. (2001) 22:1901–14.
PubMed Abstract | Google Scholar
21. Bartynski WS, Boardman JF, Zeigler ZR, Shadduck RK, Lister J., Posterior reversible encephalopathy syndrome in infection, sepsis, and shock. Am J Neuroradiol. (2006) 27:2179–90.
PubMed Abstract | Google Scholar
22. Mayama M, Uno K, Tano S, Yoshihara M, Ukai M, Kishigami Y, et al. Incidence of posterior reversible encephalopathy syndrome in eclamptic and patients with preeclampsia with neurologic symptoms. Am J Obstet Gynecol. (2016) 215:239.e1–e5. doi: 10.1016/j.ajog.2016.02.,039
PubMed Abstract | CrossRef Full Text | Google Scholar
23. McKinney AM, Short J, Truwit CL, McKinney ZJ, Kozak OS, SantaCruz KS, et al. Posterior reversible encephalopathy syndrome: incidence of atypical regions of involvement and imaging findings. Am J Roentgenol. (2007) 189:904–12. doi: 10.2214/AJR.07.2024
PubMed Abstract | CrossRef Full Text | Google Scholar
24., de Havenon A, Joos Z, Longenecker L, Shah L, Ansari S, Digre K. Posterior reversible encephalopathy syndrome with spinal cord involvement. Neurology. (2014) 83:2002–6. doi: 10.1212/WNL.0000000000001026
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Dandoy CE, Linscott LL, Davies SM, Leach JL, Myers KC, El-Bietar J, et al., Clinical utility of computed tomography and magnetic resonance imaging for diagnosis of posterior reversible encephalopathy syndrome after stem cell transplantation in children and adolescents. Biol Blood Marrow Transplant. (2015) 21:2028–32. doi: 10.1016/j.bbmt.2015.07.023
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Noda K, Fukae J, Fujishima K, Mori K, Urabe T, Hattori N, et al., Reversible cerebral vasoconstriction syndrome presenting as subarachnoid hemorrhage, reversible posterior leukoencephalopathy, and cerebral infarction. Intern Med. (2011) 50:1227–33. doi: 10.2169/internalmedicine.50.4812
CrossRef Full Text | Google Scholar
31. Doelken M, Lanz S, Rennert J, Alibek S, Richter G, Doerfler A, et al. Differentiation of cytotoxic and vasogenic edema in a patient with reversible posterior leukoencephalopathy syndrome using diffusion-weighted MRI. Diagn Interv Radiol., (2007) 13:125–8.
Google Scholar
32. Wartenberg KE, Parra A. CT and CT-perfusion findings of reversible leukoencephalopathy during triple-H therapy for symptomatic subarachnoid hemorrhage-related vasospasm. J Neuroimaging. (2006) 16:170–5. doi: 10.1111/j.1552-6569.2006.00031.x
CrossRef Full Text | Google Scholar
33. Vanacker P, Matias G, Hagmann P, Michel P., Cerebral hypoperfusion in posterior reversible encephalopathy syndrome is different from transient ischemic attack on CT perfusion. J Neuroimaging. (2015) 25:643–6. doi: 10.1111/jon.12158
CrossRef Full Text | Google Scholar
34. Lee SY, Kim SH, Lee SH, Baek HJ, Shon HS, Kim SS. Serial MR spectroscopy in relapsing reversible posterior leukoencephalopathy syndrome. Neurologist. (2009) 15:338–41. doi: 10.1097/NRL.,0b013e3181914af6
PubMed Abstract | CrossRef Full Text | Google Scholar
35. McKinney AM, Sarikaya B, Gustafson C, Truwit CL. Detection of microhemorrhage in posterior reversible encephalopathy syndrome using susceptibility-weighted imaging. Am J Neuroradiol. (2012) 33:896–903. doi: 10.3174/ajnr.A2886
PubMed Abstract | CrossRef Full Text | Google Scholar
38., Berger JR, Aksamit AJ, Clifford DB, Davis L, Koralnik IJ, Sejvar JJ, et al. PML diagnostiske kriterier: konsensus uttalelse fra AAN neuroinfectious sykdom delen. Nevrologi. (2013) 80:1430-8. doi: 10.1212/WNL.0b013e31828c2fa1
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
39. Aracki-Trenkić Og Stojanov D, Trenkić M, Radovanovic Z, Ignjatovic J, Ristic S, et al., Atypical presentation of posterior reversible encephalopathy syndrome: clinical and radiological characteristics in eclamptic patients. Bosn J Basic Med Sci. (2016) 16:180–6. doi: 10.17305/bjbms.2016.1201
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Bartynski WS, Boardman JF. Distinct imaging patterns and lesion distribution in posterior reversible encephalopathy syndrome. Am J Neuroradiol. (2007) 28:1320–7. doi: 10.3174/ajnr.,A0549
PubMed Abstract | CrossRef Full Text | Google Scholar
46. Brickman AM, Reitz C, Luchsinger JA, Manly JJ, Schupf N, Muraskin J, et al. Long-term blood pressure fluctuation and cerebrovascular disease in an elderly cohort. Arch Neurol. (2010) 67:564–9. doi: 10.1001/archneurol.2010.70
PubMed Abstract | CrossRef Full Text | Google Scholar
47., Cozzolino M, Bianchi C, Mariani G, Marchi L, Fambrini M, Mecacci F. Therapy and differential diagnosis of posterior reversible encephalopathy syndrome (PRES) during pregnancy and postpartum. Arch Gynecol Obstet. (2015) 292:1217–23. doi: 10.1007/s00404-015-3800-4
PubMed Abstract | CrossRef Full Text | Google Scholar
48. Masetti R, Cordelli DM, Zama D, Vendemini F, Biagi C, Franzoni E, et al. PRES in children undergoing hematopoietic stem cell or solid organ transplantation. Pediatrics., (2015) 135:890–901. doi: 10.1542/peds.2014-2325
CrossRef Full Text | Google Scholar