leírás
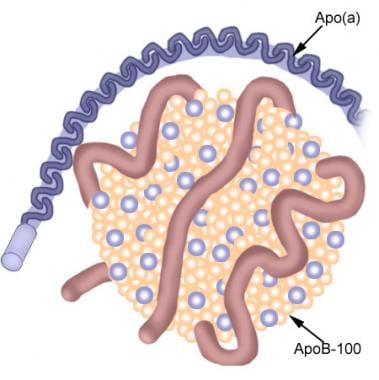 a lipoprotein(a) vázlatos rajza.
a lipoprotein(a) vázlatos rajza. annak a ténynek a következtében, hogy az Lp(a) apo(a) összetevője nagy heterogenitású komplex molekula, a plazma Lp(a) koncentrációja fordítottan függ az apo(a) méretétől. Talán nem meglepő, hogy a komplexitás ezen szintje miatt az Lp(a) több mint 25 genetikai formája létezik; így a genom fontosságát a plazmaszintek meghatározásában nem lehet túlbecsülni., Ez viszont hatással van a kardiovaszkuláris kockázat előrejelzésére a különböző populációkban.
javallatok/alkalmazások
a Koppenhágai Szívvizsgálatban Kamstrup et al megállapította, hogy az Lp(a) genetikai emelkedése a myocardialis infarctus fokozott kockázatával jár. Továbbá számos prospektív epidemiológiai vizsgálat kimutatta az Lp(a) okozati szerepét a szív-és érrendszeri betegségekben; így az Lp(a) mérése a kardiovaszkuláris kockázat meghatározójaként alkalmazható a kardiovaszkuláris kockázat globális kardiovaszkuláris kockázatértékelése keretében.,
a Muramatsu et al tanulmánya azt mutatta, hogy a koszorúér-betegségben szenvedő egyéneknél az Lp(a) magas szintjét hordozó betegeknél nagyobb a veszélyeztetett plakk formája, amelyet vékony sapkás fibroatheroma (tcfa) néven ismertek. A kutatók azt találták, hogy a TCFA a 25 mg/dL vagy annál magasabb Lp(a) szinttel rendelkező betegek 23% – ánál fordult elő, szemben a 25 mg/dL alatti Lp(a) szinttel rendelkező betegek 11% – ával.,
a Copenhagen General Population Study és a Copenhagen City Heart Study adatai alapján Langsted et al bizonyítékot talált arra, hogy az emelkedett Lp(a) plazmaszint összefüggésbe hozható a megnövekedett ischaemiás stroke kockázattal. A nyomozók arról számolt be, hogy személyek Lp(a) szint felett 93 mg/dL volt multivariable korrigált kockázati arány az ischaemiás stroke 1.60, amikor egyénekhez képest, akiknek Lp(a) szint alatt 10 mg/dL.,
Lp (A) önmagában nem ajánlott a cardiovascularis kockázat meghatározására szolgáló egyetlen vizsgálatként, hanem kiegészítő intézkedésként, amelyet a hagyományos cardiovascularis kockázati tényezők értékelésével kell kombinálni. Az Lp(a) mérése a leghasznosabb lehet közepes kockázatú betegeknél vagy azoknál, akiknél a vizsgálati eredmény befolyásolhatja az ismert kardiovaszkuláris kockázati tényezők kezelését vagy agresszivitását.,
Mint megjegyezte, Ridker Libby, bizonytalan, hogy az értékelés, Lp(a) valóban hozzáteszi prognosztikus információt, hogy teljes kockázatot az elsődleges megelőzés; azonban a legtöbb tanulmány, Lp(a) rendelkezik prediktív értéke a már ismert, hogy a magas kockázatú jelenléte miatt más kockázati tényezők, különösen a magas LDL-C szint.,
megfontolások
az Lp(a) kereskedelmi tesztjeinek szabványosítása problematikus volt az apo(a) méretétől való függőség miatt; azonban az Lp(a) méretétől függetlenül és az apo(a) méretétől függetlenül mérhető kereskedelmi vizsgálatok már számos referencialaboratóriumban elérhetők.
számos prospektív vizsgálat kimutatta, hogy az Lp(a) nemlineáris módon előre jelzi a kardiovaszkuláris kockázatot, így a kockázat növekedése meglehetősen kicsi, amíg el nem éri az Lp (a) legmagasabb szintjét(5-10%).,
az Lp(a) biomarkerként való alkalmazására vonatkozó adatok bizonyos magas kockázatú csoportokban, például krónikus vesebetegségben vagy ismert koszorúér-betegségben szenvedőknél, továbbra is ellentmondásosak.
az a megfigyelés, hogy az Lp(a) rendkívül magas szintje szinte teljes mértékben korlátozódik az egyidejűleg magas LDL-koleszterinszinttel rendelkező betegekre, megkérdőjelezi az Lp(A) alkalmazását a megnövekedett kardiovaszkuláris kockázat független markereként, és kiemeli az LDL-koleszterinnel való kölcsönhatások által bemutatott korlátozásokat.,
kevés beavatkozást találtak az Lp(a) szintek csökkentésére, a nagy dózisú niacin kivételével. A kifejezetten az Lp(a) módosítására irányuló terápia szintén ellentmondásos.
vannak feltörekvő adatok az apheresis hatékony módszerként történő alkalmazásáról az Lp(a) csökkentésére. Erre nincs gyógyszer jóváhagyva, de a legújabb vizsgálatok kimutatták, hogy az Lp(a) jelentősen csökkenthető más apolioprotein B-100(apoB) csökkenésével.