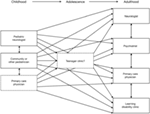
Figur 2. Skjematisk illustrerer den økende spredning av omsorg bestemmelsen etter overgang fra barn til voksen tjenester (3). Gjengitt med tillatelse fra John Libbey Eurotext.,
Andre Hensyn for LGS Management
Lennox–Gastaut syndrom pasienter er svekket i sitt daglige liv, ikke bare av en rekke typer anfall som ofte hyppige og fysisk skade (for eksempel slippe angrep), men også av en rekke alvorlige comorbidities (3). Comorbidities som er spesielt knyttet til LGS inkluderer kognitive og atferdsmessige problemer, fysisk funksjonshemming, og søvnforstyrrelser., Fem år etter LGS utbruddet, 75-95% av pasientene har kognitiv svikt (101, 102), og atferdsmessige problemer, som for eksempel hyperaktivitet, aggressivitet, og autistiske trekk, utvikle i ca 50% (10). Mobilitet er ofte sterkt påvirket av hyppige anfall (spesielt slippe angrep), som er fysisk krevende, og ofte resultere i skader (3). Pasientene har ofte å gjøre bruk av beskyttende utstyr (for eksempel en rullestol, hjelm, og/eller faceguard) for å redusere de fysiske effektene av beslag. Noen ganger bruk av verneutstyr (f.eks., gjenværende i en rullestol for å beskytte mot skader fra drop-angrep) kan i seg selv påvirke mobilitet av pasienter, mates inn i en ond sirkel som begrenser deres evne til å være fysisk aktiv. I tillegg til tidlig utvikling av dysfagi er sterkt assosiert med dårlig langvarige anfall prognose (103), og påvirker pasientenes evne til å spise og ta medisiner.
Pasienter med LGS lider søvnsyklus avbrudd på grunn av forekomsten av anfall om natten., Søvnmangel og/eller forstyrrelser påvirke den nevrofysiologiske og nevrokjemiske mekanismer som er viktige for minne-læring (104), og kan også resultere i en rekke atferdsmessige, kognitive og affektive tap ved verdifall, inkludert hyperaktivitet, redusert skolekarakterer, og depresjon (105).
Forsiktig styring av comorbidities i LGS er et sentralt aspekt av omsorg. Noen Antiepileptika kan forårsake eller forverre comorbidities (f.eks.,, kognitiv svikt, depresjon), og valg av AED behandling må derfor ta denne muligheten i betraktning, for eksempel benzodiazepiner brukes til å behandle søvnforstyrrelser kan danne utfellinger tonic beslag i LGS (106). Nøye vurdering må også tas hensyn til potensialet for AED medikament–interaksjoner med medisiner som brukes for behandling av comorbidities.,
Som en følge av den betydelige belastning av beslag og comorbidities, og bivirkningene forbundet medikamentene, QoL av LGS pasientene er svekket på mange plan (fysisk, psykisk, sosial) i hele sitt liv (3). Den fysiske virkningen av LGS, og forebyggende tiltak iverksettes for å redusere denne virkningen, alvorlig påvirke pasientenes evne til å delta i daglige aktiviteter, og oppmøte på skolen er ofte forstyrret. Kognitive og atferdsmessige problemer ofte krever spesifikke utdannings-og omsorgsbehov som vil hindre mainstream skolegang (3)., I tillegg nevnte effekten av nattlige anfall på søvn kan direkte påvirke pasientenes QoL (107). Effekten av LGS på selvstendighet, evne til å arbeide, sosial deltakelse, og personlige relasjoner fortsette å alvorlig svekke pasientenes QoL inn i voksen alder (3).,jor innvirkning på QoL av foreldre/foresatte og familier på grunn av begrensning i sosialt liv og forholdet problemer mellom partnerne og andre familiemedlemmer, og følelsen av isolasjon, noe som kan føre til depresjon, problemer med barnepass, som kan ytterligere begrense sosial deltakelse og muligheter for frist, fysisk utmattelse og/eller forstyrret søvn, angst om når beslag vil skje, vil den fremtidige utsikter for den enkelte med LGS, og de sosiale stigma forbundet med tilstanden; så vel som økonomiske problemer som følge av å gi avkall karriere utvikling i favør av omsorgssvikt (108).,
Siden LGS utgjør en stor belastning for pasienter og deres pårørende/familie, en tverrfaglig, individualisert tilnærming til omsorg er nødvendig, hvilke adresser hver pasientens medisinske, pedagogiske, psykologiske og sosiale behov i løpet av sitt liv (109). Behovene til pasienten og deres pårørende/familie bør ideelt sett være re-evalueres årlig, for å ta hensyn til faktorer som pasientens fysiske helse, deres potensielle behovet for institutionalization (spesielt i voksen alder), og støtte for pårørende/familie.,
Områder for Fremtidig Forskning
I dag, Antiepileptika er anti-beslag medisiner og derfor behandle symptomer på epilepsi, heller enn dens årsak(er). Fremtidig forskning bør fokusere på elucidating natural history av LGS og om riktig behandling kan ha en gunstig innvirkning på sin sykdomsforløpet. Dette bør ikke bare omfatte effekter av medikamentell behandling, men også den rollen kirurgiske prosedyrer, som for eksempel callosotomy., Tidlig kontroll av beslag i LGS har blitt foreslått å være assosiert med økt nevrokognitiv utfall (2), men relevansen av denne i de novo LGS, så vel som virkningen av anfall undertrykkelse i eldre barn og voksne, er mindre sikkert, og er et område som garanterer nærmere studie. Selv om oppmerksomheten er for tiden gitt til potensielle skadelige effekter av Antiepileptika på kognisjon, forskning er nødvendig for å belyse om andre ikke-AED behandlinger kan beskytte mot kognitiv svikt og/eller forbedre erkjennelse i LGS pasienter., I tillegg er forskning er nødvendig for å utvikle standardiserte verktøy for foresatte til rutinemessig måle endringer i pasientenes kognitive funksjoner og atferd over tid. Forklaring med hensyn til om det er spesifikke genotypes eller genetiske mutasjoner som avgjør en mottakelighet for LGS er også nødvendig, som kunne lede utviklingen av diagnostiske verktøy.
Gitt problemer forbundet med å telle beslag i LGS (på grunn av hyppigheten av drop-angrep, lengden på fravær beslag, etc.,), den prediktive verdien av å bruke alternative endepunkter i kliniske studier forskning bør vurderes, som for eksempel antall beslag-frie dager, snarere enn anfallsfrekvens per se. Karakterisering av faktorer som kan forutsi respons på behandling i LGS pasienter vil også være viktige i forskning og klinisk praksis innstillinger. Andre potensielle områder for fremtidig forskning inkluderer relevansen av steroid terapi i LGS, og om det kan forbedre erkjennelse , og den langsiktige virkninger av cannabidiol behandling i LGS, i form av AEs og potensial for utvikling av toleranse.,
Forfatter Bidrag
Alle forfattere (JC, SA, MF, PS, og AA) har gjort vesentlige bidrag til forståelse av denne artikkelen og analyse og tolkning av data den inneholder; var involvert i å utforme en artikkel eller revidere den kritisk for viktige intellektuelle innhold, under forutsetning av endelig godkjenning av den aktuelle versjonen til å bli publisert; og ble enige om å være ansvarlig for alle aspekter av arbeidet for å sikre at spørsmål knyttet til nøyaktigheten og integriteten til noen del av arbeidet var hensiktsmessig undersøkt og løst.,
interessekonflikt Uttalelse
JC har sittet på rådgivende komité for Eisai, UCB, Shire, Zogenix, Vitaflo, og Nutricia, for betaling og honoraria har blitt betalt til avdelingen. Hun har deltatt som etterforsker for Vitaflo, GW Pharmaceuticals, og Zogenix, med midler utbetalt til sin avdeling. Hun har også mottatt forskning midler fra Vitaflo. Hun er støttet av National Institute for Health Research Biomedical Research Centre ved Great Ormond Street Hospital for Children NHS Foundation Trust og University College London., SA har satt på rådgivende komité for Eisai, GSK, Novartis, Nutricia, Shire, Ultragenyx, og Zogenix. Han har deltatt som etterforsker for Advicenne Pharma, Eisai, UCB, Ultragenyx, og Zogenix, med midler utbetalt til hans sykehuset eller sin research lab. MF har deltatt som etterforsker for UCB, GW Pharmaceuticals, Pfizer, og LivaNova, med midler utbetalt til sin avdeling. Hun har mottatt forskning midler fra Eisai, UCB, LivaNova, og Esteve, med midler utbetalt til sin avdeling. Hun har mottatt en høyttaler honoraria fra Eisai, UCB, LivaNova, Bial, og Esteve., PS mottatt honoraria fra FB Helse, Kolfarma s.r.l., UCB Pharma, og Eisai Inc. og forskning støtte fra den italienske helsedepartementet og Telethon Foundation. AA har mottatt forskningsmidler fra Eu-Kommisjonen, UCB Pharma, og CaixaBank, med midler utbetalt til sin avdeling, og rådgivning avgifter fra Eisai, GW, Shire, Takeda, Zogenix, og UCB Pharma.
Erkjennelsene
Redaksjonell støtte til utarbeidelse av dette manuskriptet ble gitt av John Scopes av mXm Medisinsk Kommunikasjon.,
Midler
konsensus gruppe møte for utvikling av denne publikasjonen ble organisert og finansiert av Eisai Ltd. Redaksjonell støtte til utarbeidelse av denne publikasjonen ble finansiert av Eisai Ltd. De synspunktene som kommer til uttrykk i denne artikkelen, er den uavhengige konsensus synspunktene til forfatterne og har ikke vært påvirket av tredjeparts sponsing.
Forkortelser
Fotnoter
2. Arzimanoglou En, Resnick T. Alle barn som opplever epileptiske faller ikke nødvendigvis har Lennox-Gastaut syndrom… men mange gjør det., Epileptic Disord (2011) 13(Suppl 1):S3–13. doi:10.1684/epd.2011.0422
CrossRef Full Text | Google Scholar
3. Kerr M, Kluger G, Philip S. Evolution and management of Lennox-Gastaut syndrome through adolescence and into adulthood: are seizures always the primary issue? Epileptic Disord (2011) 13(Suppl 1):S15–26. doi:10.1684/epd.2011.0409
PubMed Abstract | CrossRef Full Text | Google Scholar
5., Goldsmith IL, Zupanc ML, Buchhalter JR. Long-term seizure outcome in 74 patients with Lennox-Gastaut syndrome: effects of incorporating MRI head imaging in defining the cryptogenic subgroup. Epilepsia (2000) 41(4):395–9. doi:10.1111/j.1528-1157.2000.tb00179.x
PubMed Abstract | CrossRef Full Text | Google Scholar
8. International League Against Epilepsy. Proposal for revised classification of epilepsies and epileptic syndromes., Commission on Classification and Terminology of the International League Against Epilepsy. Epilepsia (1989) 30(4):389–99. doi:10.1111/j.1528-1157.1989.tb05316.x
CrossRef Full Text | Google Scholar
10. van Rijckevorsel K. Treatment of Lennox-Gastaut syndrome: overview and recent findings. Neuropsychiatr Dis Treat (2008) 4(6):1001–19. doi:10.2147/NDT.,S1668
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Gastaut H, Dravet C, Loubier D. Evolution clinique et prognostic du syndrome de Lennox-Gastaut. In: Lugaresi E, Pazzaglia P, Tassinari CA, editors. Evolution and Prognosis of Epilepsies. Bologna, Italy: Aulo Gaggi (1973). p. 133–54.
Google Scholar
17. EuroEPINOMICS-RES Consortium, Epilepsy Phenome/Genome Project, Epi4K Consortium., De novo mutations in synaptic transmission genes including DNM1 cause epileptic encephalopathies. Am J Hum Genet (2014) 95(4):360–70. doi:10.1016/j.ajhg.2014.08.013
CrossRef Full Text | Google Scholar
18. Epilepsy Phenome/Genome Project Epi4K Consortium. Copy number variant analysis from exome data in 349 patients with epileptic encephalopathy. Ann Neurol (2015) 78(2):323–8. doi:10.1002/ana.,24457
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Larsen J, Johannesen KM, Ek J, Tang S, Marini C, Blichfeldt S, et al. The role of SLC2A1 mutations in myoclonic astatic epilepsy and absence epilepsy, and the estimated frequency of GLUT1 deficiency syndrome. Epilepsia (2015) 56(12):e203–8. doi:10.1111/epi.13222
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Hughes JR, Patil VK., Long-term electro-clinical changes in the Lennox-Gastaut syndrome before, during, and after the slow spike-wave pattern. Clin Electroencephalogr (2002) 33(1):1–7. doi:10.1177/155005940203300103
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Doose H. Myoclonic-astatic epilepsy. Epilepsy Res Suppl (1992) 6:163–8.
PubMed Abstract | Google Scholar
26. Patry G, Lyagoubi S, Tassinari CA., Subclinical «electrical status epilepticus” induced by sleep in children. A clinical and electroencephalographic study of six cases. Arch Neurol (1971) 24(3):242–52. doi:10.1001/archneur.1971.00480330070006
CrossRef Full Text | Google Scholar
28. King DW, Smith JR. Supplementary sensorimotor area epilepsy in adults. Adv Neurol (1996) 70:285–91.
PubMed Abstract | Google Scholar
29., Khan SA Carney PW, Archer JS. Kort asymmetrisk tonic posering med diffuse lav-spenning fast aktivitet i beslag fremkommer fra mesial parietal-region. Epilepsi Res (2014) 108(10):1950-4. doi:10.1016/j.eplepsyres.2014.09.011
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
33. Ohtahara S. Lennox-Gastaut syndrom. Hensyn i sitt konsept og kategorisering. Jpn J Psychiatry Neurol (1988) 42(3):535-42.,
PubMed Abstract | Google Scholar
35. Pujar S, Calvert S, Cortina-Borja M, Chin RF, Smith RA, Cross JH, et al. Statistical process control (SPC) – a simple objective method for monitoring seizure frequency and evaluating effectiveness of drug interventions in refractory childhood epilepsy. Epilepsy Res (2010) 91(2–3):205–13. doi:10.1016/j.eplepsyres.2010.07.013
CrossRef Full Text | Google Scholar
39., Morrow J, Russell A, Guthrie E, Parsons L, Robertson I, Waddell R, et al. Malformation risks of antiepileptic drugs in pregnancy: a prospective study from the UK Epilepsy and Pregnancy Register. J Neurol Neurosurg Psychiatry (2006) 77(2):193–8. doi:10.1136/jnnp.2005.074203
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Motte J, Trevathan E, Arvidsson JF, Barrera MN, Mullens EL, Manasco P, et al. Lamotrigine for generalized seizures associated with the Lennox-Gastaut syndrome., N Engl J Med (1997) 337(25):1807–12. doi:10.1056/NEJM199712183372504
CrossRef Full Text | Google Scholar
46. The Felbamate Study Group in Lennox-Gastaut Syndrome. Efficacy of felbamate in childhood epileptic encephalopathy (Lennox-Gastaut syndrome). N Engl J Med (1993) 328(1):29–33. doi:10.1056/NEJM199301073280105
CrossRef Full Text | Google Scholar
52., Ohtsuka Y, Yoshinaga H, Shirasaka Y, Takayama-R, Takano H, Iyoda K. langsiktig sikkerhet og beslag utfallet i Japanske pasienter med Lennox-Gastaut syndrom motta tilleggsbehandling rufinamide terapi: en åpen-label studier etter en randomisert klinisk studie. Epilepsi Res (2016) 121:1-7. doi:10.1016/j.eplepsyres.2016.01.002
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
55. Conry JA, Ng YT, Kernitsky L, Mitchell WG, Veidemanis R, Drummond R, et al., Stabil doser av clobazam for Lennox-Gastaut syndrom er assosiert med vedvarende drop-anfall og total-anfall forbedringer over 3 år. Epilepsia (2014) 55(4):558-67. doi:10.1111/epi.12561
CrossRef Full Tekst | Google Scholar
56. Munn R, Camfield P, Camfield C, Dooley J. Clobazam for ildfast barndom anfall – en verdifull supplerende stoff. Kan J Neurol Sci (1988) 15(4):406-8.,
Google Scholar
60. Hussain SA, Zhou R, Jacobson C, Weng J, Cheng E, Lay J, et al. Perceived efficacy of cannabidiol-enriched cannabis extracts for treatment of pediatric epilepsy: a potential role for infantile spasms and Lennox-Gastaut syndrome. Epilepsy Behav (2015) 47:138–41. doi:10.1016/j.yebeh.2015.04.009
PubMed Abstract | CrossRef Full Text | Google Scholar
62., Geffrey AL, Lyr SF, Bruno PL, Thiele EA. Drug-drug samspillet mellom clobazam og cannabidiol hos barn med refraktær epilepsi. Epilepsia (2015) 56(8):1246-51. doi:10.1111/epi.13060
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
65. Biró En, Stephani U, Tarallo T, Bast T, Schlachter K, Fleger M, et al. Effektivitet og toleranse av perampanel i barn og ungdom med ildfast epilepsies: første erfaringer. Neuropediatrics (2015) 46(2):110-6. doi:10.,1055/s-0035-1546276
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
69. Lemmon MEG, Terao NN, Ng YT, Reisig W, Rubenstein JE, Kossoff EH. Effekt av ketogen diett i Lennox-Gastaut syndrom: en retrospektiv gjennomgang av en institusjon erfaring og oppsummering av litteraturen. Dev Med Child Neurol (2012) 54(5):464-8. doi:10.1111/j.1469-8749.2012.04233.,x
PubMed Abstract | CrossRef Full Text | Google Scholar
72. Sharma S, Jain P, Gulati S, Sankhyan N, Agarwala A. Use of the modified Atkins diet in Lennox Gastaut syndrome. J Child Neurol (2015) 30(5):576–9. doi:10.1177/0883073814527162
PubMed Abstract | CrossRef Full Text | Google Scholar
76. Chambers A, Bowen JM. Electrical stimulation for drug-resistant epilepsy: an evidence-based analysis., Ont Helse Technol Vurdere Ser (2013) 13(18):1-37.
PubMed Abstrakt | Google Scholar
77. Morris GL III, Glans D, Buchhalter J, Mack KJ, Nickels K, Herde C. kunnskapsbasert retningslinje oppdatering: vagus nerve stimulering for behandling av epilepsi: rapport fra Guideline Utvikling Subcommittee of the American Academy of Neurology. Nevrologi (2013) 81(16):1453-9. doi:10.1212/WNL.,0b013e3182a393d1
CrossRef Full Text | Google Scholar
78. Karceski S. Vagus nerve stimulation and Lennox-Gastaut syndrome: a review of the literature and data from the VNS patient registry. CNS Spectr (2001) 6(9):766–70. doi:10.1017/S1092852900001516
PubMed Abstract | CrossRef Full Text | Google Scholar
84. Rolston JD, Englot DJ, Wang DD, Garcia PA, Chang EF., Corpus callosotomy versus vagus nerve stimulation for atonic seizures and drop attacks: a systematic review. Epilepsy Behav (2015) 51:13–7. doi:10.1016/j.yebeh.2015.06.001
PubMed Abstract | CrossRef Full Text | Google Scholar
86. Cukiert A, Cukiert CM, Burattini JA, Lima AM, Forster CR, Baise C, et al. Long-term outcome after callosotomy or vagus nerve stimulation in consecutive prospective cohorts of children with Lennox-Gastaut or Lennox-like syndrome and non-specific MRI findings., Beslag (2013) 22(5):396-400. doi:10.1016/j.anfall.2013.02.009
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
87. Kwan SY, Lin JH, Wong TT, Chang KP, Yiu CH. En sammenligning av anfall utfallet etter callosotomy i pasienter med Lennox-Gastaut syndrom og en positiv eller negativ historie for West syndrom. Beslag (2006) 15(7):552-7. doi:10.1016/j.anfall.2006.06.,008
PubMed Abstract | CrossRef Full Text | Google Scholar
89. Katagiri M, Iida K, Kagawa K, Hashizume A, Ishikawa N, Hanaya R, et al. Combined surgical intervention with vagus nerve stimulation following corpus callosotomy in patients with Lennox-Gastaut syndrome. Acta Neurochir (Wien) (2016) 158(5):1005–12. doi:10.1007/s00701-016-2765-9
CrossRef Full Text | Google Scholar
93. Akman CI., Nonconvulsive status epilepticus and continuous spike and slow wave of sleep in children. Semin Pediatr Neurol (2010) 17(3):155–62. doi:10.1016/j.spen.2010.06.009
PubMed Abstract | CrossRef Full Text | Google Scholar
94. Walker M, Cross H, Smith S, Young C, Aicardi J, Appleton R, et al. Nonconvulsive status epilepticus: Epilepsy Research Foundation workshop reports. Epileptic Disord (2005) 7(3):253–96.,
PubMed Abstract | Google Scholar
98. Jurasek L, Ray L, Quigley D. Development and implementation of an adolescent epilepsy transition clinic. J Neurosci Nurs (2010) 42(4):181–9. doi:10.1097/JNN.0b013e3181e26be6
PubMed Abstract | CrossRef Full Text | Google Scholar
103. Ogawa K, Kanemoto K, Ishii Y, Koyama M, Shirasaka Y, Kawasaki J, et al., Long-term follow-up studie av Lennox-Gastaut syndrom hos pasienter med alvorlige motoriske og intellektuelle funksjonshemminger: med spesiell referanse til problemet med dysfagi. Beslag (2001) 10(3):197-202. doi:10.1053/seiz.2000.0483
CrossRef Full Tekst | Google Scholar
105. O ‘ Brien LM. Den nevrokognitiv virkninger på søvn forstyrrelser hos barn og ungdom. Child Adolesc Psychiatr Clin N Am (2009) 18(4):813-23. doi:10.1016/j.chc.2009.04.,008
PubMed Abstract | CrossRef Full Text | Google Scholar
109. Arzimanoglou A, Resnick T. Diagnosing and treating epileptic drop attacks, atypical absences and episodes of nonconvulsive status epilepticus. Epileptic Disord (2011) 13(Suppl 1):S1–2. doi:10.1684/epd.2011.0408
CrossRef Full Text | Google Scholar
110. Kivity S, Lerman P, Ariel R, Danziger Y, Mimouni M, Shinnar S., Langsiktig kognitive utfall av en kohort av barn med cryptogenic infantile spasmer behandlet med høy-dose adrenocorticotropic hormon. Epilepsia (2004) 45(3):255-62. doi:10.1111/j.0013-9580.2004.30503.x
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar